题目内容
2.下列有关说法不正确的是( )| A. | C3H5Cl的链状同分异构体有4种(考虑顺反异构) | |
| B. | 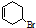 能发生氧化反应、取代反应、加成反应和消去反应 能发生氧化反应、取代反应、加成反应和消去反应 | |
| C. | 分子式符合C4H8O2的酸类和酯类同分异构体共有6种 | |
| D. | 丙烯分子内所有原子都在同一个平面 |
分析 A.CH3-CH=CHCl有顺式和反式两种结构;
B.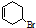 能燃烧发生氧化反应、溴原子能水解发生取代反应;
能燃烧发生氧化反应、溴原子能水解发生取代反应;
C.根据官能团异构和位置异构和碳链异构来综合分析同分异构体的种数,对于羧酸而言,根据羧基位置异构可以得到两种丁酸;根据酯基位置异构和碳链异构可得:甲酸丙酯2种(丙基2种异构)、乙酸乙酯1种、丙酸甲酯1种;
D.甲烷为空间四面体结构.
解答 解:A.由于CH3-CH=CH2 只有三种氢,所以有三种一氯代物:CH2Cl-CH=CH2、CH3-CCl=CH2、CH3-CH=CHCl,其中CH3-CH=CHCl有顺式和反式两种结构,所以分子式为C3H5Cl链状有机物的同分异构体共有4种,故A正确;
B.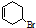 能燃烧发生氧化反应、溴原子能水解发生取代反应、双键能发生加成反应和溴原子能发生消去反应,故B正确;
能燃烧发生氧化反应、溴原子能水解发生取代反应、双键能发生加成反应和溴原子能发生消去反应,故B正确;
C.对于羧酸而言,根据羧基位置异构可以得到两种丁酸;根据酯基位置异构和碳链异构可得:甲酸丙酯2种(丙基2种异构)、乙酸乙酯1种、丙酸甲酯1种,共6种,故C正确;
D.丙烯中存在甲基,甲烷为空间四面体结构,则分子中所有原子不会在同一平面上,故D错误.
故选D.
点评 本题考查同分异构体的种类和有机物的结构与性质,根据官能团异构和位置异构和碳链异构来综合分析同分异构体的种数,难度不大,但要注意按照一定的顺序书写同分异构体.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
12.有机物可能存在同分异构现象,下列化学式只表示一种纯净物的是( )
| A. | C7H8O | B. | C3H8 | C. | C2H4Br2 | D. | C3H6O2 |
13.下列元素原子半径最大的是( )
| A. | Na | B. | Cl | C. | F | D. | Li |
10.大多数的有机物都易燃,现有如下四种物质,当质量相同的时候,在足量氧气中完全燃烧时,消耗氧气量最多的是( )
| A. | 苯 | B. | 乙烯 | C. | 异丁烷 | D. | 新戊烷 |
17.下表为元素周期表中的一部分,表中列出10种元素在周期表中的位置,按要求回答下列各题:
(1)上述10种元素中,金属性最强的元素的元素符号是K,其单质与水反应的化学方程式是2K+2H2O=2KOH+H2↑.
(2)①③⑤三种元素最高价氧化物对应水化物中碱性最强的是(填化学式)NaOH.
(3)元素①和⑦点燃时形成的化合物的化学式为Na2O2.该化合物的焰色为黄色.该化合物溶液与元素⑧的单质反应的离子方程式为2OH-+Cl2=Cl-+ClO-+H2O.
(4)②③⑤三种元素形成的离子,离子半径由大到小的顺序是K+>Mg2+>Al3+.(用微粒符号表示)
(5)元素⑧的最高价氧化物的水化物的化学式为HClO4.
(6)下列能说明氯元素比硫元素非金属性强的是:②③④.(填序号)
①硫酸比次氯酸稳定;②高氯酸是比硫酸更强的酸; ③S2-易被氯气氧化成S;
④氯化氢比硫化氢稳定; ⑤稀盐酸不跟铜反应,浓硫酸能跟铜反应.
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)①③⑤三种元素最高价氧化物对应水化物中碱性最强的是(填化学式)NaOH.
(3)元素①和⑦点燃时形成的化合物的化学式为Na2O2.该化合物的焰色为黄色.该化合物溶液与元素⑧的单质反应的离子方程式为2OH-+Cl2=Cl-+ClO-+H2O.
(4)②③⑤三种元素形成的离子,离子半径由大到小的顺序是K+>Mg2+>Al3+.(用微粒符号表示)
(5)元素⑧的最高价氧化物的水化物的化学式为HClO4.
(6)下列能说明氯元素比硫元素非金属性强的是:②③④.(填序号)
①硫酸比次氯酸稳定;②高氯酸是比硫酸更强的酸; ③S2-易被氯气氧化成S;
④氯化氢比硫化氢稳定; ⑤稀盐酸不跟铜反应,浓硫酸能跟铜反应.
7.下列有关化学用语表示正确的是( )
| A. | 次氯酸的结构式:H-Cl-O | B. | 16O2-和18O2-的结构示意图: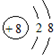 | ||
| C. | 氮气的电子式: | D. | 电子式表示氯化钠的形成过程: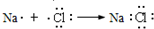 |
14.如图为元素周期表中短周期的一部分,关于Y、Z、M的说法正确的是( )
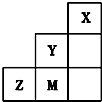

| A. | 三种元素中,Y的最高价氧化物对应的水化物酸性最强 | |
| B. | 离子半径:M->Z2->Y- | |
| C. | 稳定性:HY<HM | |
| D. | 非金属性:Y>M>Z |
11.下列实验操作中,不正确的是( )
| A. | 配制1.00mol/LNaCl溶液时,将称好的NaCl固体直接放入容量瓶中溶解 | |
| B. | 蒸馏时,冷却水从冷凝管的下口通入,上口流出 | |
| C. | 用分液漏斗分液时,下层液体从下口放出,上层液体从上口倒出 | |
| D. | 用四氯化碳萃取碘水中的碘单质 |
12.下列措施中使得水的电离平衡H2O?H++OH-正方向移动的是( )
| A. | 滴入盐酸 | B. | 滴入氢氧化钠溶液 | ||
| C. | 加热 | D. | 加水 |