题目内容
19.某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1:2,下列说法正确的是( )| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:2 | ||
| C. | 此有机物一定是烃CH4 | D. | 分子中可能含有氧原子 |
分析 有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1:2,则确定有机物分子中C、H个数之比为1:4,有机物可能是甲烷,也可能是含氧有机物.
解答 解:有机物在氧气中充分燃烧充分生成CO2和H2O的物质的量之比为1:2,
根据原子守恒可知,原有机物中的C和H的物质的量之比为1:4,
有机物可能是CH4,也可能是含氧有机物CH3OH,
故选D.
点评 本题考查有机物燃烧的计算,侧重考查学生的分析、计算能力,难度不大,注意利用原子守恒确定有机物分子中C、H原子个数之比,但不能确定是否含有氧元素.

练习册系列答案
相关题目
10.在通常条件下,下列各组物质的性质排列正确的是( )
| A. | Na、Mg、Al的第一电离能逐渐增大 | B. | 热稳定性:HF>H2O>NH3 | ||
| C. | S2-、Cl-、K+的半径逐渐增大 | D. | O、F、Ne的电负性逐渐增大 |
14.下列说法正确的是( )
| A. | 原子核都是由质子和中子构成的 | |
| B. | 不同元素原子的质量数一定不等 | |
| C. | 质子数决定元素种类,质子数和中子数决定原子种类 | |
| D. | 质子数相同的粒子,其核外电子数一定相同,但化学性质不一定相同 |
4.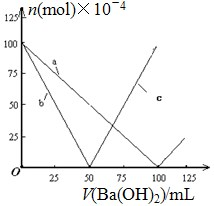 烧杯中盛有 100mL 0.1mol/L 的 NaHSO4溶液,向其中逐滴滴加 0.1mol/L 的 Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图.下列说法正确的是( )
烧杯中盛有 100mL 0.1mol/L 的 NaHSO4溶液,向其中逐滴滴加 0.1mol/L 的 Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图.下列说法正确的是( )
 烧杯中盛有 100mL 0.1mol/L 的 NaHSO4溶液,向其中逐滴滴加 0.1mol/L 的 Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图.下列说法正确的是( )
烧杯中盛有 100mL 0.1mol/L 的 NaHSO4溶液,向其中逐滴滴加 0.1mol/L 的 Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图.下列说法正确的是( )| A. | 曲线 a 表示 Ba2+的物质的量的变化 | |
| B. | 曲线 c 表示 OH-的物质的量的变化 | |
| C. | 加入 Ba(OH)2溶液 50mL 时反应的离子方程式为:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 加入 Ba(OH)2溶液大于 50mL 后,反应的离子方程式为:OH-+H+═H2O |
11.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 18g D2O所含电子数目为10NA | |
| B. | 实验室用含2molHCl的浓盐酸在加热下与足量的MnO2反应,转移的电子数为NA | |
| C. | 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为4NA | |
| D. | 标准状况下,22.4 L氦气与18g水所含分子数均为NA |
9.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 常温常压下,8.8g CO2和N2O混合物中所含有的原子数为0.6 NA | |
| B. | 二氧化锰和浓盐酸反应产生4.48L气体时,转移的电子数为0.4NA | |
| C. | 标准状况下,3.36L水中含有电子数为1.5NA | |
| D. | 在0.2mol/L的硫酸铁溶液中含有的三价铁离子数为0.6 NA |