题目内容
14.下列化学用语表示正确的是( )| A. | 乙炔球棍模型: | B. | 质量数为的37的原子${\;}_{37}^{17}$Cl | ||
| C. | 氯化镁电子式: | D. | 氯离子的结构示意图: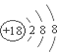 |
分析 A、乙炔为直线型结构,碳原子半径大于氢原子,据此判断乙炔的球棍模型;
B、质量数应写在原子符号的左上角;
C、氯化镁是离子化合物,由两个氯离子和一个镁离子构成;
D、氯离子的核内有17个质子.
解答 解:A、乙炔分子中含有两个碳氢键和1个碳碳三键,乙炔的球棍模型为: ,故A错误;
,故A错误;
B、质量数应写在原子符号的左上角,故质量数为37的氯原子为3717Cl,故B错误;
C、氯化镁是离子化合物,由两个氯离子和一个镁离子构成,而相同离子不能合并,故氯化镁的电子式为 ,故C正确;
,故C正确;
D、氯离子由氯原子得一个电子形成,故核内有17个质子,而核外有18个电子,故结构示意图为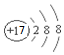 ,故D错误.
,故D错误.
故选C.
点评 本题考查了常见的化学用语的考查,难度不大,应注意的是球棍模型和比例模型的区别以及离子化合物和共价化合物电子式书写的区别.

练习册系列答案
相关题目
5.下列说法中正确的是( )
| A. | 铵盐都易溶于水 | |
| B. | 铵盐受热分解都能得到氨气 | |
| C. | 除去NH4Cl溶液中少量的CaCl2,加过量的NH4HCO3溶液后过滤 | |
| D. | 铵盐与碱液共热都能生成使蓝色石蕊试变红的气体 |
2.反应 HF(aq)+BF3(aq)=H+(aq)+BF4-(aq) 能够发生的原因是( )
| A. | 强氧化剂制弱氧化剂 | B. | 强酸制弱酸 | ||
| C. | “熵增效应(熵判据)” | D. | 产物中形成了配位键 |
9.下列关于甲、乙、丙、丁四种有机物说法正确的是( )
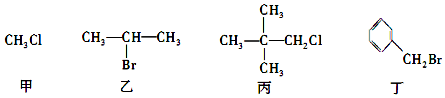
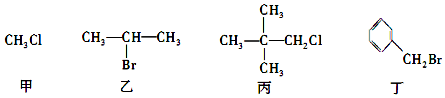
| A. | 甲、乙、丙、丁中加入NaOH的醇溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,均有沉淀生成 | |
| B. | 甲中加入NaOH的水溶液共热,再滴入AgNO3溶液,可检验该物质中含有的卤素原子 | |
| C. | 乙发生消去反应得到两种烯烃 | |
| D. | 丙与NaOH的水溶液共热,反应后生成的醇能被氧化为醛 |
6.关于如图所示装置的叙述,错误的是( )
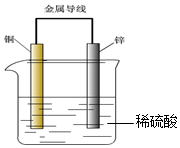

| A. | 锌是负极,随着放电的进行其质量逐渐减轻 | |
| B. | 放电过程中氢离子移向铜极,硫酸根离子移向锌极 | |
| C. | 电流从锌极经导线流向铜极 | |
| D. | 锌极上发生的是氧化反应,铜极上发生的是还原反应 |
3.下列有关说法错误的是( )
| A. | 磷原子的质子数为14 | B. | 氧元素在第二周期 | ||
| C. | 氯元素的最高化合价为+7 | D. | 还原性 Na<K |