题目内容
3.若某体系所吸收的热量全部用于体系的内能增加,则所需的条件是( )①封闭体系;②不做体积功其他功;③恒压;④恒温.
| A. | ②和④ | B. | ①和③ | C. | ①和② | D. | ①和④ |
分析 首先是封闭系统,否则内能增加过程中必然对外有热损失,其次是不做体积功其他功,吸收的热量全部转化为物质内能;
解答 解:若某体系所吸收的热量全部用于体系的内能增加,必须是密闭体系,其次是不做体积功其他功,可以满足体系所吸收的热量全部用于体系的内能增加,
故①②正确,
故选C.
点评 本题考查了物质内能转化的条件分析,注意题目是吸收的热量全部用于体系的内能增加,体积不变,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.NA为阿伏加德罗常数,则下列说法正确的是( )
| A. | 已知C2H2(g)+$\frac{5}{2}$O2(g)→2CO2(g)+H2O(l)△H=-1300KJ/mol 当有5NA个电子转移时能放出650KJ的热量 | |
| B. | 有28g乙烯与丙烯混合气体,其含原子总数为3NA个 | |
| C. | 有反应H2(g)+I2(g)?2HI(g)△H=-QHJ/mol在298K 101KPa下向一密闭容器中充入NA个H2和NA个I2,充分反应共放出热量为QKJ | |
| D. | 在78g苯中含3NA个碳碳双键 |
11.氮的氢化物NH3、N2H4等在工农业生产、航空航天等领域有广泛应用.
(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势.氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2(g)═4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)═5N2(g)+6H2O(l)△H2
则反应 4NH3(g)+3O2(g)═2N2(g)+6H2O(l)△H=$\frac{3△H{\;}_{1}+2△H{\;}_{2}}{5}$.(请用含有△H1、△H2的式子表示)
(2)合成氨实验中,在体积为3L的恒容密闭容器中,投入4mol N2和9mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
已知:破坏1mol N2(g)和3mol H2(g)中的化学键吸收的总能量小于形成2mol NH3(g)中的化学键放出的总能量.①则T1<T2(填“>”、“<”或“=”)
②在T2时,经过10min达到化学平衡状态,则0至10min内H2的平均反应速率v(H2)=0.1mol•L-1•min-1,平衡时N2的转化率α(N2)=25%.
③下列图象分别代表焓变(△H)、混合气体平均相对分子质量($\overline{M}$)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是BC.

(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势.氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2(g)═4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)═5N2(g)+6H2O(l)△H2
则反应 4NH3(g)+3O2(g)═2N2(g)+6H2O(l)△H=$\frac{3△H{\;}_{1}+2△H{\;}_{2}}{5}$.(请用含有△H1、△H2的式子表示)
(2)合成氨实验中,在体积为3L的恒容密闭容器中,投入4mol N2和9mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
| 温度(K) | 平衡时NH3的物质的量(mol) |
| T1 | 2.4 |
| T2 | 2.0 |
②在T2时,经过10min达到化学平衡状态,则0至10min内H2的平均反应速率v(H2)=0.1mol•L-1•min-1,平衡时N2的转化率α(N2)=25%.
③下列图象分别代表焓变(△H)、混合气体平均相对分子质量($\overline{M}$)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是BC.

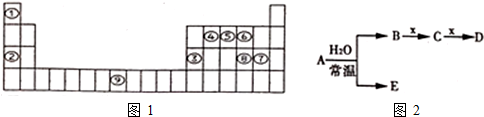
18.四种短周期元素在周期表中的相对位置如下所示,其中Z元素最外层电子数是其电子层数的2倍.下列说法正确的是( )
| X | Y | |
| Z | W |
| A. | 四种短周期元素中W的原子半径最小 | |
| B. | Z元素在周期表中的位置是第三周期第ⅣA族 | |
| C. | 原子最外层电子数由多到少的顺序:Y>X>W>Z,最高正价由高到低顺序:W>Z | |
| D. | 元素非金属性由强到弱的顺序:W>Z,W的单质常温下可与氢氧化钠溶液反应 |
7.短周期五种非金属元素甲、乙、丙、丁、戊在元素周期表中的相对位置如图所示.下列判断正确的是( )
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A. | 原子半径:甲<乙,简单阴离子的半径:丙>丁>戊 | |
| B. | 非金属性:乙<丁 | |
| C. | 最高价氧化物对应的水化物的酸性:丙<丁 | |
| D. | 气态氢化物的稳定性:丙>丁>戊 |
17.设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1mol甲醇中含有C-H键的数目为4NA | |
| B. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| C. | 0.1mol的CaC2中含阴离子数是0.1NA | |
| D. | 1L 0.1mol•L-1的NaHCO3溶液中HCO${\;}_{3}^{-}$和CO${\;}_{3}^{2-}$离子数之和为0.1NA |
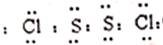 .
.