题目内容
下列说法正确的是( )
| A、强电解质导电能力一定强 |
| B、含强极性键的共价化合物一定是强电解质 |
| C、强电解质的饱和溶液一定是浓溶液 |
| D、强电解质的水溶液中一定存在电离平衡 |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:A.溶液的导电能力与溶液中离子浓度成正比,与电解质的强弱无关;
B.H-S键为极性共价键,但氯化氢为弱电解质;
C.硫酸钡是强电解质,其饱和溶液是极稀溶液;
D.水溶液中存在水的电离平衡.
B.H-S键为极性共价键,但氯化氢为弱电解质;
C.硫酸钡是强电解质,其饱和溶液是极稀溶液;
D.水溶液中存在水的电离平衡.
解答:
解:A.强电解质导电能力不一定强,溶液的导电能力与溶液中离子浓度成正比,与电解质的强弱无关,故A错误;
B.含强极性键的共价化合物不一定是强电解质,如H2S,H-S键为极性共价键,但氯化氢为弱电解质,故B错误;
C.强电解质的饱和溶液不一定是浓溶液,如硫酸钡的饱和溶液是极稀溶液,故C错误;
D.水溶液中存在水的电离平衡,故D正确,
故选D.
B.含强极性键的共价化合物不一定是强电解质,如H2S,H-S键为极性共价键,但氯化氢为弱电解质,故B错误;
C.强电解质的饱和溶液不一定是浓溶液,如硫酸钡的饱和溶液是极稀溶液,故C错误;
D.水溶液中存在水的电离平衡,故D正确,
故选D.
点评:本题考查电解质溶液的导电能力、水的电离平衡、电解质的溶解性等,难度不大.要注意平时知识的积累.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列举措不符合“节能减排”要求的是( )
| A、在西部和沿海地区兴建风力发电站,解决能源问题 |
| B、推广与发展小排量汽车和电动、混合动力汽车 |
| C、大力开发丰富的煤炭资源,减少对石油的依赖 |
| D、回收废弃饮料包装纸,制作成公园内的休闲长椅 |
下列各组物质的性质比较中,不正确的是( )
| A、金属性强弱:Na>Mg>Al |
| B、氢化物稳定性:HF>H2O>NH3 |
| C、碱性强弱:KOH>NaOH>LiOH |
| D、酸性强弱:HIO4>HBrO4>HClO4 |
下列各个装置中能组成原电池的是( )
A、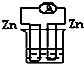 稀硫酸 |
B、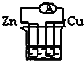 CuSO4溶液 |
C、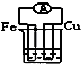 酒精溶液 |
D、 |
下列变化不属于氧化还原反应的是( )
| A、2HClO═2HCl+O2↑ | ||||
| B、2Na2O2+2CO2═2Na2CO3+O2 | ||||
| C、4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||||
D、2NaHCO3
|
可逆反应3H2+N2?2NH3达到平衡的标志是( )
①消耗3mol H2的同时生成2mol NH3
②1个N≡N键断裂的同时,有3个H-H键形成
③H2、N2与NH3的物质的量之比为3:1:2
④1个N≡N键断裂的同时,有6个N-H键断裂
⑤1个N≡N键断裂的同时,有6个N-H键形成.
①消耗3mol H2的同时生成2mol NH3
②1个N≡N键断裂的同时,有3个H-H键形成
③H2、N2与NH3的物质的量之比为3:1:2
④1个N≡N键断裂的同时,有6个N-H键断裂
⑤1个N≡N键断裂的同时,有6个N-H键形成.
| A、①②⑤ | B、②④ |
| C、①②③④ | D、全部 |
下列实验操作中叙述正确的是( )
| A、萃取操作必须在分液漏斗中进行 |
| B、漏斗、试管、蒸馏烧瓶、天平、分液漏斗、研钵常用于物质分离 |
| C、用剩的药品均不能放回原试剂瓶中 |
| D、分液时,分液漏斗内下层液体从下口放出,上层液体从上口倒出 |
下列溶液中的Cl-浓度与100mL 1mol/L MgCl2溶液中的Cl-浓度相等的是( )
| A、150 mL 1mol/LNaCl溶液 |
| B、75mL 1mol/L CaCl2溶液 |
| C、150 mL 0.2mol/LKCl溶液 |
| D、75mL 1mol/LAlCl3溶液 |
铜锌原电池(如图)工作时,下列叙述正确的是( )
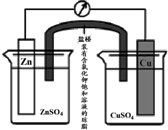

| A、在外电路中,电流从Zn极流向Cu极 |
| B、盐桥中的Cl-移向CuSO4溶液 |
| C、当负极减小65g时,正极增加65g |
| D、电池的总反应为 Zn+Cu2+=Zn2++Cu |