题目内容
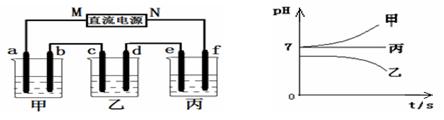
某兴趣小组利用如图所示装置进行实验。
(1)断开K2、闭合K1,U形管内除电极上有气泡外,还可观察到的现象是 ;阳极电极反应式为 。当电路中转移0.001mol电子时,右侧注射器最多可以收集到气体 mL(折算为标准状况)。
(2)断开K2、闭合K1一段时间,待注射器中充有一定量的气体后,断开K1、闭合K2,此时装置内化学能转化为电能。实现能量转化的化学方程式为 ;
(3)假设实验装置不漏气,当(2)中注射器内气体全部参加反应后,U形管内的溶液理论上 (填“能”或“不能”)恢复原样。
(1)有白色沉淀生成 2Cl- - 2e-=Cl2↑ 11.2 (2)H2+Cl2=2HCl (3)能
解析试题分析:(1)若断开K2、闭合K1,该装置为电解池。左边的石墨电极为阳极,右边的石墨电极为阴极。在阳极由于放电能力Cl->OH-,所以发生反应:2Cl—2e-=Cl2↑。在阴极由于放电能力H+>Mg2+,因此在阴极发生反应:2H++2e-=H2↑。H+不断放电,破坏了附近的水的电离平衡,水继续电离。最终使附近的水溶液显碱性。这时会发生反应:Mg2+ +2OH-=Mg(OH)2↓.因此在U形管内除电极上有气泡外,还可观察到有白色沉淀生成。当电路中转移0.001mol电子时,根据电子守恒可知右侧注射器收集的H2的物质的量为0.0005mol.其在标准状况下的体积为0.0005mo×22.4L/mol=0.0112L=11.2ml.(2)若断开K2、闭合K1,发生的的电解池反应,左边收集的是Cl2,右边收集的是H2。此时断开K1、闭合K2,装置内就实现化学能转化为电能。即发生了原电池反应。实现能量转化的化学方程式为H2+Cl2=2HCl。(3)假设实验装置不漏气,当(2)中注射器内气体全部参加反应后,根据能量守恒定律,U形管内的溶液理论上能恢复原样。
考点:考查电解池、原电池的反应原理及应用的知识。

 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案如下图所示,用铅蓄电池电解100 g 10.0%的硫酸钠溶液,经过一段时间后,测得溶液质量变为95.5 g。下列说法正确的是( )
| A.电路中转移0.25 mol电子 |
| B.铅蓄电池中消耗0.5 mol H2SO4 |
| C.铅蓄电池的负极反应式为:PbSO4+2H2O-2e-=PbO2+4H++SO |
| D.Fe电极发生的电极反应为Fe-2e-=Fe2+ |