题目内容
7.某研究性学习小组利用手持技术探究强碱和不同的酸中和反应的过程如下:(1)实验步骤:
①分别配制浓度均为0.mol•L-1的NaOH、HCl、CH3COOH溶液备用.配制过程中用到玻璃仪器有量筒、烧杯、容量瓶、玻璃棒、细口瓶、胶头滴管
②在锥形瓶中加入l0mL0.1mol•L-1的HCl,在25.00mL碱式(填“酸式”、“碱式”)滴定管中加入0.1mol•L-1的NaOH,连接数据采集器和pH传感器.
③向锥形瓶中滴入NaOH,接近估算的NaOH用量附近时,减慢滴加速度,等读数稳定后,再滴下一滴NaOH.
④存储计算机绘制的pH变化图.用0.1 mol•L-1的CH3COOH溶液代替HCl重复上述②~④的操作.
(2)结果分析:
20℃时NaOH分别滴定HCl、CH3COOH的pH变化曲线如下.
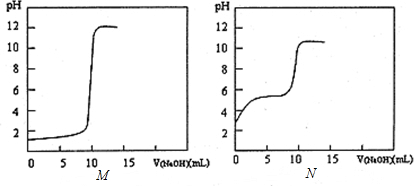
根据上述曲线回答下列问题:
①其中表示滴定盐酸的曲线是M(填“M”或“N”).
②则20℃时该浓度醋酸中已电离的量与初始总量之比为1:100.
③当滴定至两溶液的pH均为8时,两溶液中c(Na+)关系为M>(填“<”“>”或“=”).
分析 (1)①根据溶液的配制过程选择仪器;
②NaOH溶液应该用碱式滴定管量取;
(2)①常温下0.1mol•L-1的HCl溶液的pH=1;
②根据醋酸未滴定前溶液的pH确定溶液里H+浓度;
③依据依据完全中和时溶液的pH情况及盐类水解分析;
解答 解:(1)①根据溶液的配制过程选择仪器,在定容时需要胶头滴管,故答案为:胶头滴管;
②NaOH溶液能腐蚀酸式滴定管中的活塞,所以要用碱式滴定管,故答案为:碱式;
(2)①图M显示未滴定前溶液的pH=1,0.1mol•L-1的HCl溶液的pH=1,则M曲线为测定盐酸的曲线,故答案为:M;
②图N为滴定醋酸的曲线,未滴定前醋酸溶液的pH为3,即溶液里H+浓度为0.001mol/L,则20℃时该浓度醋酸中已电离的量与初始总量之比为0.001mol/L:0.1mol/L=1:100,故答案为:1:100;
③酸碱完全中和需要的NaOH溶液均为10.00mL,此时NaCl溶液的pH=7显中性,而CH3COONa溶液因CH3COO-的水解显碱性,此时溶液pH约为8,故滴定HCl溶液里需要继续滴加一定量的NaOH才可以使溶液的pH达到8,则两溶液中c(Na+)关系为M>N,故答案为:>.
点评 本题考查了中和滴定实验,以及弱酸的电离,盐类的水解,难度中等,要注意滴定管的选择.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.有A、B、C、D四瓶溶液,它们是硫酸钠,亚硫酸钠、盐酸和氯化钡溶液.为了鉴别它们,各取少量溶液进行两两反应,结果如表所示,表中“↓”表示有沉淀或微溶物质生成,“↑”表示有气体生成,“-”表示无明显现象.由此可以推断它们的组成为:AHCl;BBaCl2;CNa2SO4;DNa2SO3.
| A | B | C | D | |
| A | - | - | ↑ | |
| B | - | ↓ | ↓ | |
| C | - | ↓ | - | |
| D | ↑ | ↓ | - |
19.已知35Cl是质子数为17,相对原子质量为35的氯原子;37Cl是指质子数为17,相对原子质量为37的氯原子.反应K35ClO3+6H37Cl═KCl+3Cl2↑+3H2O,有关叙述正确的是( )
| A. | KCl中含有35Cl | |
| B. | 生成物Cl2的平均相对分子质量为73.3 | |
| C. | 1molK35ClO3参加反应,失去电子数为5NA | |
| D. | 氧化剂和还原剂的物质的量之比1:6 |
19.下列装置不可用于NH3的尾气吸收的是( )
| A. | 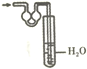 | B. |  | C. | 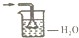 | D. | 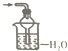 |
16.下列各组离子能够大量共存的是( )
| A. | Na+、Ca2+、Cl-、NO3- | B. | Fe2+、H+、SO32-、ClO- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、Fe3+、NO3-、SCN- |
17.以下化学方程式中水只作为氧化剂的是( )
| A. | NaH+H2O═NaOH+H2↑ | B. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ | ||
| C. | F2+H2O═2HF+O2↑ | D. | Cl2+H2O?HCl+HClO |
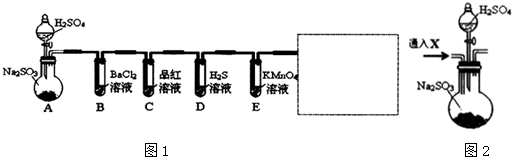
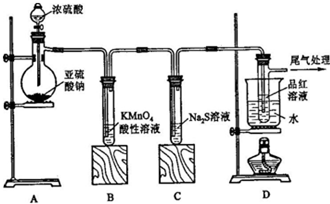
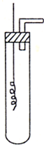 某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置.请你根据他们的思路,选择下列药品完成实验,填写实验步骤并回答问题.供选择的药品:铜丝、稀硝酸、烧碱溶液、铁粉、CaCO3颗粒.
某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置.请你根据他们的思路,选择下列药品完成实验,填写实验步骤并回答问题.供选择的药品:铜丝、稀硝酸、烧碱溶液、铁粉、CaCO3颗粒.