题目内容
16. 实验室常用如图所示装置制取少量乙酸乙酯.请回答下列问题:
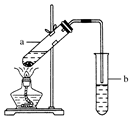
实验室常用如图所示装置制取少量乙酸乙酯.请回答下列问题:(1)试管a中需加入浓硫酸、乙酸各2mL,乙醇3mL,应该先加入乙醇,再加入浓硫酸,最后加入乙酸.
(2)试管a中发生反应的化学方程式是CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,反应类型是酯化(取代)反应,通常加入几片碎瓷片,其作用是防暴沸.
(3)试管b中加入饱和Na2CO3溶液,其作用是反应掉挥发出来的乙酸;溶解挥发出来的乙醇;减小乙酸乙酯的溶解度,使溶液分层,便于得到乙酸乙酯.
(4)反应结束后,振荡试管b,静置.观察到的现象试管b中的液体分层,上层是透明的油状液体.
分析 a种乙醇和乙酸在浓硫酸作用下发生酯化反应生成乙酸乙酯,实验时应先加乙醇,后加浓硫酸,最后加乙酸,试管b中碳酸钠溶液可吸收乙醇、除去乙酸,降低乙酸乙酯的溶解度,加热可加快反应速率,长导管可冷凝回流,充分利用原料,以此来解答.
解答 解:(1)试管a中需要加入浓硫酸、冰醋酸和乙醇各2mL,正确的加入顺序及操作是先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,最后再加入冰醋酸,
故答案为:乙醇;浓硫酸;乙酸;
(2)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应为:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,液体乙酸乙醇沸点低,加热要加碎瓷片,防止暴沸,
故答案为:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O;酯化(取代)反应;防暴沸;
(3)试管b中加有饱和Na2CO3溶液,其作用是反应掉挥发出来的乙酸;溶解挥发出来的乙醇;减小乙酸乙酯的溶解度,使溶液分层,便于得到乙酸乙酯,
故答案为:反应掉挥发出来的乙酸;溶解挥发出来的乙醇;减小乙酸乙酯的溶解度,使溶液分层,便于得到乙酸乙酯;
(4)反应结束后,振荡试管b,静置.观察到的现象是b中的液体分层,上层是透明的油状液体,
故答案为:试管b中的液体分层,上层是透明的油状液体.
点评 本题考查有机物的制备实验,为高频考点,把握制备实验操作、混合物分离提纯、有机物的性质为解答的关键,侧重分析与实验能力的考查,注意实验安全的分析,题目难度不大.

练习册系列答案
相关题目
3.某兴趣小组制备氢氧化亚铁沉淀.
(1)实验1中产生白色沉淀的离子方程式是Fe2++2OH-=Fe(OH)2↓.
(2)为了探究沉淀变灰绿色的原因,该小组同学展开如下探究:
①甲同学推测灰绿色物质为Fe(OH)2和Fe(OH)3混合物.查阅资料后根据调色原理认为白色和红褐色的调和色不可能是灰绿色,并设计实验证实灰绿色物质中不含有Fe(OH)3,方案是取一定量的灰绿色沉淀,加入盐酸溶解,再加入KSCN溶液,若溶液不变红色,则证明灰绿色物质中不含有Fe(OH)3.
②乙同学查阅文献:Fe(OH)2在大量SO42-存在的情况下形成Fe6(SO4)2(OH)4O3(一种氧基碱式复盐).并设计对比实验证实该假设:向试管中加入2mL0.1mol/LFeCl2溶液,再往试管中加入3滴0.1mol/LNaOH溶液,振荡,现象与实验1相同,结论是该假设不成立.
③乙同学继续查阅文献:Fe(OH)2沉淀具有较强的吸附性能,灰绿色可能是由Fe(OH)2表面吸附Fe2+引起.推测所用的硫酸亚铁溶液的浓度应越小越好;氢氧化钠溶液浓度应越大越好.设计了如下实验方案:
该实验得出的结论是在氢氧化钠溶液浓度一定的条件下,硫酸亚铁溶液的浓度越小,产生白色沉淀的现象越明显,能说明灰绿色是由Fe(OH)2表面吸附Fe2+引起的证据是实验2中沉淀下沉后,大部分灰绿色变为白色沉淀(或实验3中沉淀下沉后,底部都为白色沉淀).丙同学认为该实验方案不足以证明灰绿色是由Fe(OH)2表面吸附Fe2+引起的,还需补充的实验是向实验2(或实验3)的白色沉淀中继续加入过量的硫酸亚铁溶液,白色沉淀变成灰绿色,证明该假设成立.
(3)丙同学探究温度对氢氧化亚铁制备实验的影响:取少量灰绿色沉淀,在水浴中加热,颜色由灰绿变白,且有絮状白色沉淀下沉,原因为Fe2+在加热时易发生水解,生成Fe(OH)2,因此颜色变白,同时沉淀的量增加,导致出现絮状白色沉淀.
(4)根据以上实验探究,若尽可能制得白色Fe(OH)2沉淀,需要控制的实验条件隔绝氧气、硫酸亚铁少量(或氢氧化钠过量)、硫酸亚铁浓度小(或氢氧化钠浓度大)、将氢氧化钠溶液逐滴加入到硫酸亚铁溶液中、微热等.
| 实验1 | 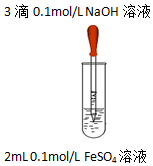 | 实验现象 |
| 液面上方产生白色絮状沉淀,迅速变为灰绿色,振荡,试管壁上有红褐色沉淀生成. |
(2)为了探究沉淀变灰绿色的原因,该小组同学展开如下探究:
①甲同学推测灰绿色物质为Fe(OH)2和Fe(OH)3混合物.查阅资料后根据调色原理认为白色和红褐色的调和色不可能是灰绿色,并设计实验证实灰绿色物质中不含有Fe(OH)3,方案是取一定量的灰绿色沉淀,加入盐酸溶解,再加入KSCN溶液,若溶液不变红色,则证明灰绿色物质中不含有Fe(OH)3.
②乙同学查阅文献:Fe(OH)2在大量SO42-存在的情况下形成Fe6(SO4)2(OH)4O3(一种氧基碱式复盐).并设计对比实验证实该假设:向试管中加入2mL0.1mol/LFeCl2溶液,再往试管中加入3滴0.1mol/LNaOH溶液,振荡,现象与实验1相同,结论是该假设不成立.
③乙同学继续查阅文献:Fe(OH)2沉淀具有较强的吸附性能,灰绿色可能是由Fe(OH)2表面吸附Fe2+引起.推测所用的硫酸亚铁溶液的浓度应越小越好;氢氧化钠溶液浓度应越大越好.设计了如下实验方案:
| 试管中10mL NaOH溶液 | 滴加 FeSO4溶液 | 实验现象 | |
| 实验2 | 6mol/L NaOH溶液 | 0.2mol/L FeSO4溶液 | 产生悬浮于液面的白色沉淀(带有少量灰绿色),沉淀下沉后,大部分灰绿色变为白色沉淀 |
| 实验3 | 6mol/L NaOH溶液 | 0.1mol/L FeSO4溶液 | 产生悬浮于液面的白色沉淀(带有极少量灰绿色),沉淀下沉后,底部都为白色沉淀 |
(3)丙同学探究温度对氢氧化亚铁制备实验的影响:取少量灰绿色沉淀,在水浴中加热,颜色由灰绿变白,且有絮状白色沉淀下沉,原因为Fe2+在加热时易发生水解,生成Fe(OH)2,因此颜色变白,同时沉淀的量增加,导致出现絮状白色沉淀.
(4)根据以上实验探究,若尽可能制得白色Fe(OH)2沉淀,需要控制的实验条件隔绝氧气、硫酸亚铁少量(或氢氧化钠过量)、硫酸亚铁浓度小(或氢氧化钠浓度大)、将氢氧化钠溶液逐滴加入到硫酸亚铁溶液中、微热等.
7.下列实验操作正确的是( )
| A. | 用量筒量取25.00mL蒸馏水 | B. | 用分液漏斗分离乙醇和水 | ||
| C. | 用烧杯溶解FeCl3试样 | D. | 用托盘天平称量NaCl固体5.80g |
8.等体积等浓度的MOH强碱溶液和HA弱酸溶液混合后,混合液中有关离子的浓度应满足的关 系是( )
| A. | [M+]>[OH-]>[A-]>[H+] | B. | [M+]>[A-]>[H+]>[OH-] | C. | [M+]>[A-]>[OH-]>[H+] | D. | [M+]>[H+]=[A-]>[OH-] |
5.将等物质的量的SO2、Cl2通入水中,所得的溶液( )
| A. | 具有中性漂白性 | B. | 具有酸性漂白性 | C. | 只有漂白性 | D. | 只有酸性 |
6.药物阿司匹林可由水杨酸制得,它们的结构如图所示.有关说法正确的是( )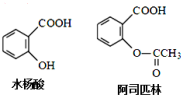

| A. | 1 mol阿司匹林最多可消耗3 molH2 | |
| B. | 水杨酸分子中所有原子不可能共面 | |
| C. | 水杨酸可以发生取代、加成、氧化、加聚反应 | |
| D. | 1 mol阿司匹林最多可消耗2 molNaOH |
 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.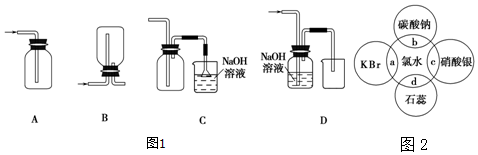
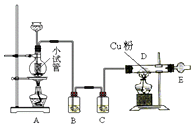 如图是用干燥纯净的Cl2与Cu粉反应来制取无水氯化铜的实验装置图,请回答下列问题:
如图是用干燥纯净的Cl2与Cu粉反应来制取无水氯化铜的实验装置图,请回答下列问题: