题目内容
| |||||||||||||||||||
答案:3.1:9;
解析:
解析:
(1) |
10-14,10-12,温度升高,水的电离程度增大,则溶液中的H+和OH-浓度增大,从而导致KW增大 |
(2) |
c(Na+)>c(A-)>c(OH-)>c(H+) |
(4) |
pH酸+pH碱=13 |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
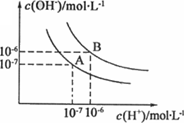
 水的电离平衡曲线如右图所示,下列说法不正确的是( )
水的电离平衡曲线如右图所示,下列说法不正确的是( )
