题目内容
据科学家预测,月球的土壤中吸附着数百万吨的
He,每百吨
He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上,氦元素主要以
He的形式存在.下列说法正确的是( )
3 2 |
3 2 |
4 2 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
考点:质量数与质子数、中子数之间的相互关系,同位素及其应用
专题:
分析:根据原子符号ZAX的含义,A表示质量数,Z表示质子数.
A.元素符号的左下角为质子数;
B.中子数=质量数-质子数;
C.质子数相同,中子数不同的原子互称为同位素;
D.当第一层是最外层时,2个电子是稳定结构.
A.元素符号的左下角为质子数;
B.中子数=质量数-质子数;
C.质子数相同,中子数不同的原子互称为同位素;
D.当第一层是最外层时,2个电子是稳定结构.
解答:
解:A.24He原子核内含有2个质子,故A错误;
B.23He中子数=3-2=1,故B错误;
C.23He和24He质子数相同,中子数不同,故互为同位素,故C正确;
D.因He原子的结构稳定,既不容易得到电子,也不容易失去电子,性质不活泼,故D错误;
故选C.
B.23He中子数=3-2=1,故B错误;
C.23He和24He质子数相同,中子数不同,故互为同位素,故C正确;
D.因He原子的结构稳定,既不容易得到电子,也不容易失去电子,性质不活泼,故D错误;
故选C.
点评:本题主要考查了原子符号的含义、核素的种类以及同位素的概念,难度不大,明确概念是解答本题关键.

练习册系列答案
相关题目
已知:①Cl2+KBr═2KCl+Br2;②KClO3+6HCl═3Cl2↑+KCl+3H2O;③2KBrO3+Cl2═Br2+2KClO3,下列说法正确的是( )
| A、上述三个反应都有单质生成,所以都是置换反应 |
| B、氧化性由强到弱的顺序是KBrO3>KClO3>Cl2>Br2 |
| C、反应②中还原剂与氧化剂的物质的量之比为6:1 |
| D、反应③中1mol还原剂参加反应时氧化剂得到电子的物质的量为2 mol |
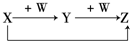 X、Y、Z、W有如图所示的转化关系,则X、W可能是( )
X、Y、Z、W有如图所示的转化关系,则X、W可能是( )①C、O2 ②AlCl3、NaOH ③Fe、HNO3 ④CO2、NaOH.
| A、①②③ | B、①② |
| C、③④ | D、①②③④ |
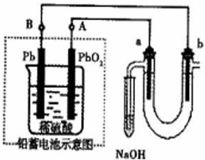 用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中正确的是 ( )(填序号)
用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中正确的是 ( )(填序号)| A、铅蓄电池负极的反应式为:Pb-2e-=Pb2+ |
| B、铅蓄电池放电时,B极质量减轻,A极质量增加 |
| C、铅蓄电池充电时,A极应与外电源负极相连 |
| D、电解苦卤水时,a电极首先放电的是Br- |
下列实验操作中错误的是( )
| A、蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、称量NaOH固体时,将NaOH固体放在托盘天平的左盘的烧杯中 |
甲、乙、丙、丁分别是Na2CO3、AgNO3、BaCl2、盐酸四种无色溶液中的一种,它们两两反应后的现象如下:甲+乙→沉淀;甲+丙→沉淀;乙+丙→沉淀;丙+丁→沉淀;乙+丁→无色无味气体.则甲、乙、丙、丁四种溶液依次是( )
| A、BaCl2、Na2CO3、AgNO3、盐酸 |
| B、BaCl2、Na2CO3、盐酸、AgNO3 |
| C、Na2CO3、盐酸、AgNO3、BaCl2 |
| D、AgNO3、盐酸、BaCl2、Na2CO3 |
下列实验设计和结论相符的是( )
A、加入NaOH溶液并加热,能产生使湿润红色石蕊试纸变蓝的气体,则一定含有N
| ||
| B、将SO2通入溴水,溴水褪色,说明SO2具有漂白性 | ||
| C、某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42- | ||
| D、在含FeCl2杂质的FeCl3溶液中通入足量Cl2后,充分加热除去过量的Cl2,即可得到较纯净的FeCl3溶液 |
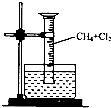 某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.请回答有关问题:
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.请回答有关问题: