题目内容
(14分)有机物A((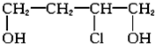 ))是合成高分子化合物HPMA的中间体,HPMA可用于制备锅炉阻垢剂。关于A有如下反应流程:
))是合成高分子化合物HPMA的中间体,HPMA可用于制备锅炉阻垢剂。关于A有如下反应流程:
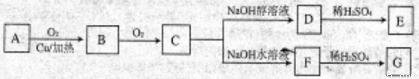
请回答下列问题:
(1)有机物A不能够发生的反应有:_________(填写字母)
A. 取代反应 B. 加成反应 C. 消去反应 D. 酯化反应
(2)可与1mol 有机物C反应的NaOH的物质的量最多可为___________
A. 1mol B. 2mol C. 3mol D. 4mol
(3)1mol A与E可在浓硫酸作用下脱去2mol H2O,写出该反应的化学方程式:________________;
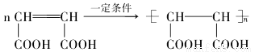
(4)E在高温、高压和催化剂作用下反应生成高分子化合物HPMA,写出该反应的化学方程式:________;
(5)H是G的一种同分异构体。0.1mol H与足量金属Na反应放出3.36L氢气(标准状况下),0.1mol H足量NaHCO3反应放出2.24LCO2(标准状况下),H能发生银镜反应。H的结构简式可能是:____________、________________.
(1)B (2)C;
(3 )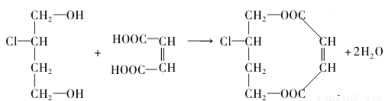 ;
;
(4) ;
;
(5)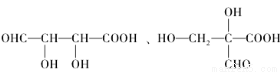
【解析】
试题分析:(1)由于在有机物A中含羟基,所以可以发生取代反应、酯化反应,由于在羟基连接的C原子的邻位C原子上有H原子或在Cl原子连接的C原子的邻位C原子上有H原子,所以可以发生消去反应,由于在物质的分子中无碳碳双键,所以不能发生加成反应。因此有机物A不能够发生的反应有B. 加成反应;(2)有机物A催化氧化得到B:OHC-CH2-CHCl-CHO;B再催化氧化得到C:HOOC-CH2-CHCl-COOH;在C的分子中含有两个羧基和一个Cl原子,因此可与1mol 有机物C反应的NaOH的物质的量最多可为3mol的NaOH,因此选项是C;(3)C与NaOH的乙醇溶液发生消去反应和酸碱中和反应产生D:NaOOC-CH=CH-COONa;D与稀硫酸发生反应产生E:HOOC-CH=CH-COOH;1mol A与E可在浓硫酸作用下脱去2mol H2O,该反应的化学方程式是: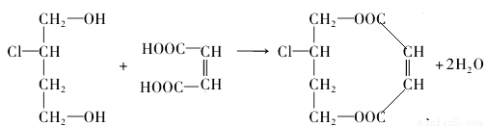 ;(4)E在高温、高压和催化剂作用下反应生成高分子化合物HPMA,该反应的化学方程式是:
;(4)E在高温、高压和催化剂作用下反应生成高分子化合物HPMA,该反应的化学方程式是: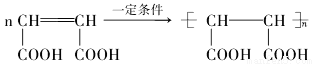 ;(5)C:HOOC-CH2-CHCl-COOH;与NaOH的水溶液发生取代反应和酸碱中和反应,产生F: NaOOC-CH2-CH(OH)-COONa;F与稀硫酸发生复分解反应产生G:HOOC-CH2-CH(OH)-COOH。H是G的一种同分异构体,0.1mol H与足量金属Na反应放出3.36L氢气(标准状况下),则H中含有三个羟基(包括醇羟基和羧基羟基),0.1mol H与足量NaHCO3反应放出2.24LCO2(标准状况下),则H中含有2个羧基和一个醇羟基,H能发生银镜反应,则H中含有醛基。H的结构简式可能是:
;(5)C:HOOC-CH2-CHCl-COOH;与NaOH的水溶液发生取代反应和酸碱中和反应,产生F: NaOOC-CH2-CH(OH)-COONa;F与稀硫酸发生复分解反应产生G:HOOC-CH2-CH(OH)-COOH。H是G的一种同分异构体,0.1mol H与足量金属Na反应放出3.36L氢气(标准状况下),则H中含有三个羟基(包括醇羟基和羧基羟基),0.1mol H与足量NaHCO3反应放出2.24LCO2(标准状况下),则H中含有2个羧基和一个醇羟基,H能发生银镜反应,则H中含有醛基。H的结构简式可能是: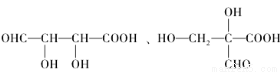 。
。
考点:考查有机物的结构、性质、转化、化学方程式、同分异构体的种类及书写的知识。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案已知25。C时,下表为几种常见物质的溶度积常数;下列有关说法不正确的是( )
化学式 | 溶度积常数 | 化学式 | 溶度积常数 |
Ag2S | 6.3×10-50 | AgCl | 1.8×10-10 |
CuS | 4.3×10-36 | AgBr | 5.4×10-13 |
FeS | 6.3×10-18 | AgI | 8.3×10-17 |
A.除去工业废水中的Cu2+可以选用Na2S作沉淀剂
B.将AgCl、AgBr和AgI饱和溶液等体积混合后,再加入足量的浓AgNO3溶液,首先析出AgI沉淀
C.Ag2S、CuS、FeS溶解度依次增大
D.将FeS加入较浓的CuSO4溶液中,会有CuS生成
 键和
键和 键的个数之比为__________(填最简整数比);
键的个数之比为__________(填最简整数比); 2C3(g);△H =-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达平衡后C3的浓度为w mol/L,放出热量b kJ。
2C3(g);△H =-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达平衡后C3的浓度为w mol/L,放出热量b kJ。