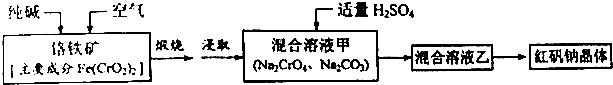
题目内容
8.4.0g硫粉在O2中完全燃烧生成SO2,放出37kJ热量,计算S的燃烧热.分析 4g硫粉完全燃烧生成二氧化硫气体,放出37kJ的热量,所以32g硫粉完全燃烧生成二氧化硫气体,放出296kJ的热量,则热化学方程式为:S(s)+O2(g)═SO2(g),△H=-296kJ/mol,依据热化学方程式和燃烧热概念可知S的燃烧热,由此分析解答.
解答 解:4g硫粉完全燃烧生成二氧化硫气体,放出37kJ的热量,所以32g硫粉完全燃烧生成二氧化硫气体,放出296kJ的热量,则热化学方程式为:S(s)+O2(g)═SO2(g),△H=-296kJ/mol,依据热化学方程式和燃烧热概念可知,S的燃烧热为296kJ/mol,答:S的燃烧热为:296kJ/mol.
点评 本题主要考查燃烧热的计算,反应热的数值与化学方程式前面的系数成正比,题目难度不大.

练习册系列答案
相关题目
16.下图是CH4、CCl4、CH3Cl的分子球棍模型图,下列说法正确的是( )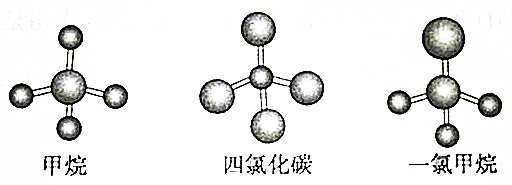

| A. | CH4、CCl4和CH3Cl都是正四面体结构 | |
| B. | CH4、CCl4都是正四面体结构 | |
| C. | CH4和CCl4中的化学键均为非极性键 | |
| D. | CH4、CCl4的结构相同,性质也相同 |
3.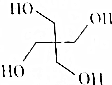 季戊四醇被大量用于涂料工业生产醇酸树脂、合成高级润滑剂、增塑剂、表面活性剂以及医药、炸药等,其结构简式如图所示.季戊四醇可由HCHO与CH3CHO两种有机物按一定比例加成得到的产物与H2再加成得到.则反应中HCHO与CH3CHO的物质的量之比为( )
季戊四醇被大量用于涂料工业生产醇酸树脂、合成高级润滑剂、增塑剂、表面活性剂以及医药、炸药等,其结构简式如图所示.季戊四醇可由HCHO与CH3CHO两种有机物按一定比例加成得到的产物与H2再加成得到.则反应中HCHO与CH3CHO的物质的量之比为( )
 季戊四醇被大量用于涂料工业生产醇酸树脂、合成高级润滑剂、增塑剂、表面活性剂以及医药、炸药等,其结构简式如图所示.季戊四醇可由HCHO与CH3CHO两种有机物按一定比例加成得到的产物与H2再加成得到.则反应中HCHO与CH3CHO的物质的量之比为( )
季戊四醇被大量用于涂料工业生产醇酸树脂、合成高级润滑剂、增塑剂、表面活性剂以及医药、炸药等,其结构简式如图所示.季戊四醇可由HCHO与CH3CHO两种有机物按一定比例加成得到的产物与H2再加成得到.则反应中HCHO与CH3CHO的物质的量之比为( )| A. | 1:1 | B. | 1:2 | C. | 3:1 | D. | 3:2 |
4.某二元甘油酯可以看成是甘油(丙三醇)与一元羧酸反应的产物,符合条件的甘油酯共有15种,则一元羧酸最少有( )
| A. | 五种 | B. | 两种 | C. | 三种 | D. | 四种 |
8.A.B.C是周期表中相邻的三个元素,A和B是同周期,B和C同主族,三种元素最外层电子总数之和为17,核内质子数之和为31,则A.B.C三种元素是( )
| A. | Mg、Al、B | B. | Li、Be、Mg | C. | N、O、S | D. | O、F、C |
9.已知X、Y、Z三种元素的为同一周期的元素,且它们的最高价氧化物对应的水化物酸性依次增强,则下列判断不正确的是( )
| A. | 原子半径按X、Y、Z的顺序增大 | B. | 原子序数按X、Y、Z顺序增大 | ||
| C. | 单质的氧化性按X、Y、Z顺序增强 | D. | 氢化物的稳定性按X、Y、Z顺序增强 |

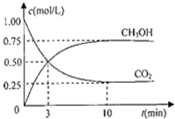 甲醇(CH3OH)是一种优质燃料,
甲醇(CH3OH)是一种优质燃料,