题目内容
在500mL CuSO4和Fe2(SO4)3的混合液中加入21.7g铁粉,待反应完全后,得到16.8g残留固体.在滤液中加入400mL 4mol?L-1的BaCl2溶液,恰好使溶液中的SO
完全沉淀.求原混合液中CuSO4和Fe2(SO4)3的物质的量浓度.
2- 4 |
考点:有关混合物反应的计算
专题:计算题
分析:原溶液中n(SO42-)=n(BaCl2)=0.4L×4mol/L=1.6mol,
假设原溶液中只有CuSO4,由Fe+Cu2+=Cu+Fe2+可知,则参加反应的n(Fe)=n(CuSO4)=1.6mol,反应的铁粉质量为:1.6mol×56g/mol=89.6g,
假设原溶液中只有Fe2(SO4)3,由Fe+Fe2(SO4)3=3FeSO4可知,则参加反应的n(Fe)=1.6mol×
,反应的铁粉质量为:1.6mol×
×56g/mol=22.9g,
所以21.7g铁粉会完全反应,没有剩余,最后得到16.8g残留固体为铜,
因氧化性Fe3+>Cu2+,则加入铁粉,先发生Fe+Fe2(SO4)3=3FeSO4,Fe3+反应完毕后发生Fe+CuSO4=FeSO4+Cu,根据方程式计算生成16.8gCu消耗Fe的质量,进而计算与Fe2(SO4)3反应消耗Fe的质量,根据方程式计算n[Fe2(SO4)3],再根据硫酸根守恒计算n(CuSO4),根据c=
计算它们的浓度.
假设原溶液中只有CuSO4,由Fe+Cu2+=Cu+Fe2+可知,则参加反应的n(Fe)=n(CuSO4)=1.6mol,反应的铁粉质量为:1.6mol×56g/mol=89.6g,
假设原溶液中只有Fe2(SO4)3,由Fe+Fe2(SO4)3=3FeSO4可知,则参加反应的n(Fe)=1.6mol×
| 1 |
| 3 |
| 1 |
| 3 |
所以21.7g铁粉会完全反应,没有剩余,最后得到16.8g残留固体为铜,
因氧化性Fe3+>Cu2+,则加入铁粉,先发生Fe+Fe2(SO4)3=3FeSO4,Fe3+反应完毕后发生Fe+CuSO4=FeSO4+Cu,根据方程式计算生成16.8gCu消耗Fe的质量,进而计算与Fe2(SO4)3反应消耗Fe的质量,根据方程式计算n[Fe2(SO4)3],再根据硫酸根守恒计算n(CuSO4),根据c=
| n |
| V |
解答:
解:原溶液中n(SO42-)=n(BaCl2)=0.4L×4mol/L=1.6mol,
假设原溶液中只有CuSO4,由Fe+Cu2+=Cu+Fe2+可知,则参加反应的n(Fe)=n(CuSO4)=1.6mol,反应的铁粉质量为:1.6mol×56g/mol=89.6g,
假设原溶液中只有Fe2(SO4)3,由Fe+Fe2(SO4)3=3FeSO4可知,则参加反应的n(Fe)=1.6mol×
,反应的铁粉质量为:1.6mol×
×56g/mol=22.9g,
所以21.7g铁粉会完全反应,没有剩余,最后得到16.8g残留固体为铜,
Fe+CuSO4=FeSO4+Cu
56 64
m(Fe) 16.8g
m(Fe)=
=14.7g
与Fe2(SO4)3反应的铁粉质量为21.7g-14.7g=7g,
Fe+Fe2(SO4)3=3FeSO4
56g 1mol
7g n[Fe2(SO4)3]
所以 n[Fe2(SO4)3]=
=0.125mol,
故c故原溶液中c[Fe2(SO4)3]=
=0.25mol/L,
根据硫酸根守恒,则n(CuSO4)=1.6mol-0.125mol×3=1.225mol,则c(CuSO4)=
=2.45mol/L,
答:原混合液中CuSO4为2.45mol/L,Fe2(SO4)3为0.25mol/L.
假设原溶液中只有CuSO4,由Fe+Cu2+=Cu+Fe2+可知,则参加反应的n(Fe)=n(CuSO4)=1.6mol,反应的铁粉质量为:1.6mol×56g/mol=89.6g,
假设原溶液中只有Fe2(SO4)3,由Fe+Fe2(SO4)3=3FeSO4可知,则参加反应的n(Fe)=1.6mol×
| 1 |
| 3 |
| 1 |
| 3 |
所以21.7g铁粉会完全反应,没有剩余,最后得到16.8g残留固体为铜,
Fe+CuSO4=FeSO4+Cu
56 64
m(Fe) 16.8g
m(Fe)=
| 16.8g×56 |
| 64 |
与Fe2(SO4)3反应的铁粉质量为21.7g-14.7g=7g,
Fe+Fe2(SO4)3=3FeSO4
56g 1mol
7g n[Fe2(SO4)3]
所以 n[Fe2(SO4)3]=
| 7g×1mol |
| 56g |
故c故原溶液中c[Fe2(SO4)3]=
| 0.125mol |
| 0.5L |
根据硫酸根守恒,则n(CuSO4)=1.6mol-0.125mol×3=1.225mol,则c(CuSO4)=
| 1.225mol |
| 0.5L |
答:原混合液中CuSO4为2.45mol/L,Fe2(SO4)3为0.25mol/L.
点评:本题考查混合物计算,难度中等,判断残留固体的成分是关键,注意硫酸铜不一定完全反应.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
NO与NO2的混合气体60ml,通入水中,最后收集到的气体体积为40ml(气体体积均在相同条件下测定),则原混合气体中NO与NO2的体积比为( )
| A、1:2 | B、2:3 |
| C、3:2 | D、1:1 |
化学与科技、社会、生产密切结合,下列有关说法不正确的是( )
| A、“乙醇汽油”的广泛使用能有效减少有害气体的排放 |
| B、向鸡蛋白溶液中缓慢加入饱和(NH4)2SO4溶液有沉淀产生属于物理变化 |
| C、“无氟冰箱”取代“含氟冰箱”,对臭氧层起到了保护作用 |
| D、从油菜籽中提取的生物柴油与从石油炼制得到的柴油都属于烃类物质 |
下列气体物质的主要来源及对环境影响相对应的是( )
| 气体物质 | 主要来源 | 对环境的影响 | |
| A | 二氧化碳 | 化石燃料的燃烧 | 酸雨 |
| B | 二氧化硫 | 汽车尾气的排放 | 光化学烟雾 |
| C | 二氧化氮 | 工厂废气的排放 | 温室效应 |
| D | 甲醛 | 各类含酚醛树脂胶的人造板装饰材料 | 室内空气污染 |
| A、A | B、B | C、C | D、D |
下列叙述正确的是( )
| A、电解精炼金属时,含杂质的粗金属做阳极,与电源正极相连 |
| B、电解池中金属导线中电子由电源的负极流向电解池的阳极,从电解池的阴极流向电源的正极 |
| C、在电解池中,电解质溶液中的阴离子向阴极移动,阳离子向阳极移动 |
| D、在电解精炼金属过程中,电解质溶液的成分不发生任何变化 |
将两个铂电极插入500mL CuSO4溶液中进行电解,通电一定时间后,某一电极增重0.064g(设电解时该电极无氢气析出,且不考虑水解和溶液体积变化).此时溶液中氢离子浓度约为( )
| A、4×l0-3 mol/L |
| B、2×l0-3 mol/L |
| C、1×l0-3 mol/L |
| D、1×l0-7 mol/L |
将盛有1mol NO和NO2的混合气体的试管倒立于水槽中,再通入0.4mol O2,充分反应后,水便会充满整个试管.则原混合气体中NO与NO2体积比为( )
| A、1:2 | B、2:5 |
| C、3:7 | D、无法确定 |
下列能达到实验目的是( )
A、 防倒吸 |
B、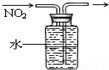 排水法收集NO2 |
C、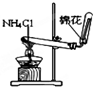 实验室制氨气 |
D、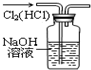 除去杂质气体HCl |
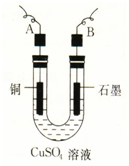 某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(m g)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,所用部分仪器及装置如图所示,回答下列问题:
某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(m g)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,所用部分仪器及装置如图所示,回答下列问题: