题目内容
18.下列物质的水溶液因水解而呈碱性的是( )| A. | NaCl | B. | NH4Cl | C. | Na2CO3 | D. | NaOH |
分析 盐的水溶液因水解而呈碱性,说明该盐属于强碱弱酸盐,NaClA为强酸强碱盐、氯化铵为强酸弱碱盐、氢氧化钠为强碱,只有碳酸钠为强碱弱酸盐,据此进行解答.
解答 解:A.NaCl在溶液中不水解,其溶液为中性,故A错误;
B.NH4Cl为强酸弱碱盐,铵根离子在溶液中水解,溶液呈酸性,故B错误;
C.Na2CO3为强碱弱酸盐,碳酸根离子水解,溶液呈碱性,满足条件,故C正确;
D.NaOH为强碱溶液,不满足条件,故D错误;
故选C.
点评 本题考查了盐的水解的应用,题目难度不大,明确盐的水解原理为解答关键,注意掌握盐的类型及溶液性质,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.下列说法不正确的是( )
| A. | 硅胶可用作食品干燥剂 | |
| B. | 蚕丝、人造丝充分水解后均可得倒氨基酸 | |
| C. | 海水提溴过程中有氧化还原反应发生 | |
| D. | 燃料的脱硫、脱氮都是减少酸雨产生的措施 |
9.解释下列实验事实的离子方程式正确的是( )
| A. | 向稀Fe(NO3)2和NaBr混合溶液加入少量稀盐酸:6Br-+8H++2NO${\;}_{3}^{-}$═3Br2+2NO↑+4H2O | |
| B. | 往NH4Al(SO4)2溶液中滴加Ba(OH)2溶液加热,刚好使NH4+全部转化为NH3:NH4++Al3++SO42-+Ba2+4OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+Al(OH)3↓+BaSO4+H2O | |
| C. | 碳酸钠溶液呈碱性:CO32-+2H2O?H2CO3+2OH- | |
| D. | 用氢氧化钠溶液去除铝条表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O |
3.下列说法不正确的是( )
| A. | 126C和146C是一种核素 | |
| B. | 红磷和白磷互为同素异形体 | |
| C. | CH3COOCH2CH3和CH3CH2COOCH3是不同物质 | |
| D. | CH3CH2OH可看成是由-C2H5和-OH两种基团组成 |
10.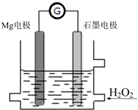 Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下.下列说法不正确的是( )
Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下.下列说法不正确的是( )
 Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下.下列说法不正确的是( )
Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下.下列说法不正确的是( )| A. | 石墨电极是该电池的正极 | |
| B. | 石墨电极上发生还原反应 | |
| C. | Mg电极的电极反应式:Mg-2e-=Mg2+ | |
| D. | 电池工作时,电子从Mg电极经导线流向石墨电极,再出石墨电极经电解质溶液流向Mg电极 |
7.下列说法不正确的是( )
| A. | 常温下,在0.10mol•L-1CH3COOH溶液中加入少量CH3COONa晶体,能使CH3COOH的电离度降低,溶液的pH增大 | |
| B. | 常温下向氯化铵溶液中加入少量氨水使溶液中c(NH4+)=c(Cl-),则混合液的pH=7 | |
| C. | 已知草酸氢钾溶液呈酸性,则在0.1 mol•L-1KHC2O4溶液中c(C2O42-)>c(K+)>c(H2C2O4) | |
| D. | pH=3的0.1 mol•L-1HA溶液与0.05 mol•L-1NaOH溶液等体积混合后所得溶液中:2c(H+)+c(HA)=c(A-)+2c(OH-) |
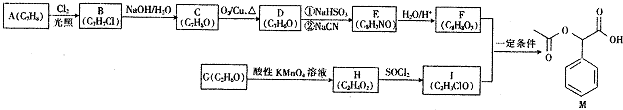
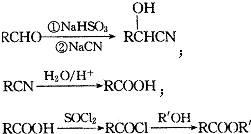 ;
;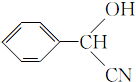 ;
; ;
;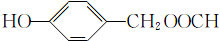 (填结构简式).
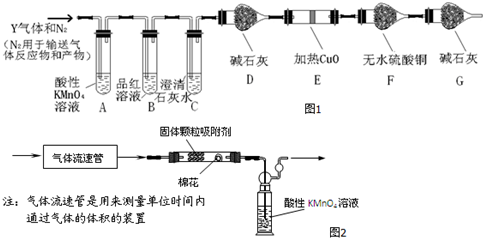
(填结构简式).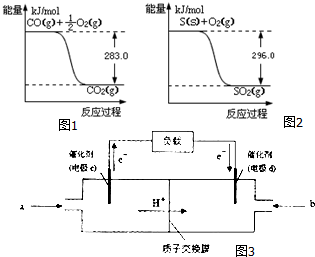 一氧化碳是一种用途广泛的化工基础原料.有机物加氢反应中镍是常用的催化剂.但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2,为弄清该方法对催化剂的影响,查得资
一氧化碳是一种用途广泛的化工基础原料.有机物加氢反应中镍是常用的催化剂.但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2,为弄清该方法对催化剂的影响,查得资