题目内容
钠铝合金(常温液态)可作为核反应堆的载热介质.下列说法正确的是( )
| A、该合金的熔点高于金属钠的熔点 |
| B、若将钠铝合金投入水中得到无色溶液且无固体剩余,则n(Al)>n(Na) |
| C、若将钠铝合金投入FeCl3溶液中有Fe(OH)3沉淀生成 |
| D、等质量的钠铝合金中铝的含量越大,与足量盐酸反应时放出的氢气越少 |
考点:有关混合物反应的计算
专题:
分析:A.合金的熔点低于其任一成分熔点;
B.该反应方程式为:Na+Al+2H2O=NaAlO2+2H2↑,根据方程式判断;
C.Na和水反应生成NaOH,NaOH溶液和FeCl3发生复分解反应;
D.根据金属钠和金属铝和酸反应生成氢气量的关系:
Al~H2↑,2Na~H2↑判断.
B.该反应方程式为:Na+Al+2H2O=NaAlO2+2H2↑,根据方程式判断;
C.Na和水反应生成NaOH,NaOH溶液和FeCl3发生复分解反应;
D.根据金属钠和金属铝和酸反应生成氢气量的关系:
| 2 |
| 3 |
解答:
解:A.合金的熔点低于其任一成分熔点,所以该合金的熔点低于金属钠的熔点,故A错误;
B.该反应方程式为:Na+Al+2H2O=NaAlO2+2H2↑,根据方程式知,若将钠铝合金投入水中得到无色溶液且无固体剩余,则n(Na)≥n(Al),故B错误;
C.Na和水反应生成NaOH,NaOH溶液和FeCl3发生复分解反应生成氢氧化铁红褐色沉淀,故C正确;
D.根据
Al~H2↑,2Na~H2↑知,11g钠放出2g氢气,9g铝就可以放出2g氢气,所以相同质量的钠铝合金中铝含量越大,放出氢气越多,故D错误;
故选C.
B.该反应方程式为:Na+Al+2H2O=NaAlO2+2H2↑,根据方程式知,若将钠铝合金投入水中得到无色溶液且无固体剩余,则n(Na)≥n(Al),故B错误;
C.Na和水反应生成NaOH,NaOH溶液和FeCl3发生复分解反应生成氢氧化铁红褐色沉淀,故C正确;
D.根据
| 2 |
| 3 |
故选C.
点评:本题以钠铝合金为载体考查了合金的性质及物质之间的反应,明确物质的性质是解本题关键,根据钠、铝与氢气之间的关系式及钠铝之间的关系式来分析解答,题目难度中等.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
某透明的溶液中加入铝粉能放出氢气,此溶液中一定能大量共存的离子组是( )
| A、K+、Cu2+、Cl-、SO42- |
| B、HCO3-、NO3-、SO42-、Na+ |
| C、Cl-、SO42-、K+、Na+ |
| D、Na+、SO42-、Cl-、AlO2- |
向一定量的Fe、FeO、Fe2O3的混合物中加入100mL浓度为1.0mol?L-1的盐酸,恰好使混合物完全溶解,有气体放出,所得溶液中加入KSCN溶液后无血红色出现.若用足量的CO在高温下还原相同质量此混合物,能得到铁的质量是( )
| A、11.2g | B、5.6g |
| C、2.8g | D、1.4g |
已知25℃时,氢氟酸的电离平衡常数KaHF=3.6×10-4,CaF2的溶度积常数Ksp(CaF2)=1.46×10-10,现向1L 0.2mol?L-1HF溶液中加入1L 0.2mol?L-1CaCl2溶液,则下列说法中,正确的是( )
| A、25℃时,0.1mol?L-1HF 溶液中pH=2 |
| B、Ksp(CaF2)随温度和浓度的变化而变化 |
| C、该体系中没有沉淀产生 |
| D、该体系中HF与CaCl2反应产生沉淀 |
下列分子中的所有原子都在同一平面的是( )
| A、环己烷 | B、溴苯 | C、丙烯 | D、丁炔 |
 在一定条件下,N2(g)+3H2(g)?2NH3(g)△H=-93.0kJ?mol-1,
在一定条件下,N2(g)+3H2(g)?2NH3(g)△H=-93.0kJ?mol-1,

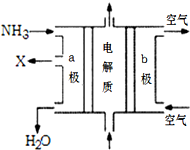 以下是对化学反应变化过程及结果的研究.按要求回答问题:
以下是对化学反应变化过程及结果的研究.按要求回答问题: