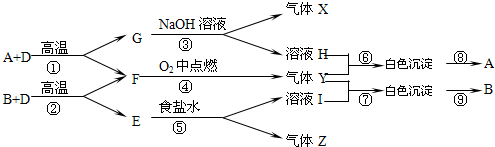
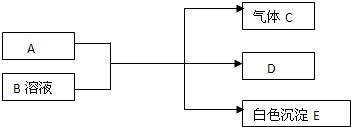
题目内容
对于平衡体系mA(g)+nB(g)?pC(g)+qD(g);△H<0.下列结论中正确的是( )
| A、若温度不变,将容器的体积增大1倍,此时A的浓度变为原来的0.48倍,则m+n>p+q | ||
| B、若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n | ||
| C、若m+n=p+q,则往含有a mol气体的平衡体系中再加入b mol B,达到新平衡时,气体的总物质的量等于(a+b) | ||
D、温度不变时,若压强增大至原来的2倍,达到新平衡时,总体积一定是原体积的
|
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A.若温度不变,将容器的体积增大1倍,若平衡不移动,A的浓度为原来的一半,而此时A的浓度为原来的0.48倍,则增大体积平衡正向移动;
B.A、B 的转化率相等,则起始量之比等于化学计量数之比;
C.若m+n=p+q,反应前后气体的总物质的量不变,则再加amolB,平衡后气体总物质的量等于amol混合气体与amolB的物质的量之和;
D.pV=nRT可知,温度不变,由压强增大到原来的2倍,若m+n=p+q,平衡可能不移动.
B.A、B 的转化率相等,则起始量之比等于化学计量数之比;
C.若m+n=p+q,反应前后气体的总物质的量不变,则再加amolB,平衡后气体总物质的量等于amol混合气体与amolB的物质的量之和;
D.pV=nRT可知,温度不变,由压强增大到原来的2倍,若m+n=p+q,平衡可能不移动.
解答:
解:A.若温度不变,将容器的体积增大1倍,若平衡不移动,A的浓度为原来的一半,而此时A的浓度为原来的0.48倍,则增大体积平衡正向移动,即增大体积,压强减小,平衡向气体体积增大的方向移动,所以m+n<p+q,故A错误;
B.A、B 的转化率相等,则起始量之比等于化学计量数之比,即反应开始时,A、B的物质的量之比为m:n,故B正确;
C.若m+n=p+q,反应前后气体的总物质的量不变,则再加amolB,平衡后气体总物质的量等于amol混合气体与amolB的物质的量之和,则达到新平衡时,气体的总物质的量等于2a mol,故C正确;
D.pV=nRT可知,温度不变,由压强增大到原来的2倍,若m+n=p+q,平衡可能不移动,所以达到新平衡时,总体积可能等于原来的
,故D错误,
故选BC.
B.A、B 的转化率相等,则起始量之比等于化学计量数之比,即反应开始时,A、B的物质的量之比为m:n,故B正确;
C.若m+n=p+q,反应前后气体的总物质的量不变,则再加amolB,平衡后气体总物质的量等于amol混合气体与amolB的物质的量之和,则达到新平衡时,气体的总物质的量等于2a mol,故C正确;
D.pV=nRT可知,温度不变,由压强增大到原来的2倍,若m+n=p+q,平衡可能不移动,所以达到新平衡时,总体积可能等于原来的
| 1 |
| 2 |
故选BC.
点评:本题考查化学平衡的影响因素,注意对于反应前后气体体积不变的反应压强改变不会引起平衡移动,把握化学计量数的关系、压强对平衡的影响为解答的关键,选项D为易错点,题目难度不大.

练习册系列答案
相关题目
下列实验装置或操作(已略去部分夹持仪器)正确的是( )
A、 配置溶液 |
B、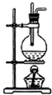 实验室制乙烯 |
C、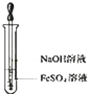 制备Fe(OH)2 |
D、 制备与收集氨气 |
 简单原子的原子结构可用图形象地表示:其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的组合是( )
简单原子的原子结构可用图形象地表示:其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的组合是( )a.①②③互为同位素
b.①②③互为同素异形体
c.①②③是三种化学性质不同的粒子
d.①②③具有相同的质量数
e.①②③具有相同的质量
f.①②③是三种不同的原子.
| A、a、f | B、b、c |
| C、d、e | D、e、f |
下列各组离子能够大量共存的是( )
| A、K+、Al3+、Cl-、AlO2- |
| B、Fe2+、Mg2+、SO42-、NO3- |
| C、Fe3+、K+、SO42-、S2- |
| D、Na+、Ca2+、OH-、HCO3- |
氢化热是指一定条件下,1mol不饱和化合物加氢时放出的热量.表中是环己烯( )、环己二烯(
)、环己二烯(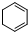 )和苯的氢化热数据:
)和苯的氢化热数据:
根据表中数据推断正确的是( )
 )、环己二烯(
)、环己二烯( )和苯的氢化热数据:
)和苯的氢化热数据:| 物质 | 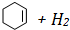 | 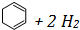 |  |
| 氢化热(kJ/mol) | 119.7 | 232.7 | 208.4 |
| A、环己二烯与H2的反应最剧烈 |
| B、环己烯、环己二烯和苯有相同的官能团 |
| C、三种化合物中环己二烯的稳定性最强 |
D、上述条件下,1 mo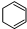 转变 转变 为时放出热量 为时放出热量 |
某种氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A、氯元素的相对原子质量是
| ||
B、m g该氯原子的物质的量是
| ||
| C、该氯原子的摩尔质量是17aNAg/mol | ||
| D、a g该氯原子所含质子数是17NA |
荧光棒发光的原理是利用H2O2氧化草酸酯产生能量,该能量传递给荧光物质而发光.草酸酯是一种粘稠度较高的有机化合物.下列说法不正确的是( )
| A、荧光棒发光,凑近可燃性气体,会导致气体燃烧 |
| B、当荧光棒亮度减弱时,敲打荧光棒亮度可能增强 |
| C、荧光棒放入冷冻室亮度可能减弱甚至消失 |
| D、荧光棒发光是化学能转化为热能,热能转化为光能 |