题目内容
下列水解离子方程式表达正确的是( )
分析:A.水解为可逆反应;
B.水解为可逆反应,且水解程度小,不生成沉淀;
C.碳酸根离子水解分步进行,以第一步为主;
D.铵根离子水解生成一水合氨和氢离子.
B.水解为可逆反应,且水解程度小,不生成沉淀;
C.碳酸根离子水解分步进行,以第一步为主;
D.铵根离子水解生成一水合氨和氢离子.
解答:解:A.NaAc的溶液中水解离子反应为Ac-+H2O?HAc+OH-,故A错误;
B.AlCl3的溶液中水解离子反应为Al3++3H2O?Al(OH)3+3H+,故B错误;
C.Na2CO3的溶液的水解离子反应为CO32-+H2O?HCO3-+OH-,故C错误;
D.NH4Cl的溶液中的水解离子反应为NH4++H2O?NH3?H2O+H+,故D正确;
故选:D.
B.AlCl3的溶液中水解离子反应为Al3++3H2O?Al(OH)3+3H+,故B错误;
C.Na2CO3的溶液的水解离子反应为CO32-+H2O?HCO3-+OH-,故C错误;
D.NH4Cl的溶液中的水解离子反应为NH4++H2O?NH3?H2O+H+,故D正确;
故选:D.
点评:本题考查离子反应方程式的书写,为高考常见题型,明确水解为可逆反应及弱酸根离子水解特点即可解答,侧重水解离子反应的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁[Fe(OH)SO4]的工艺流程如下:
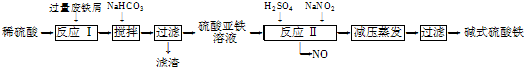
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
回答下列问题:
(1)加入少量NaHCO3的目的是调节pH,使溶液中的 (填“Fe3+”“Fe2+”或“Al3+”)沉淀,该工艺中“搅拌”的作用是 .
(2)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作 .若参与反应的O2有11.2L(标准状况),则相当于节约NaNO2的物质的量为 .
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)
聚合离子.该水解反应的离子方程式为 .
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO
.为检验所得产品中是否含有Fe2+,应使用的试剂为 (填字母).
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液.

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)加入少量NaHCO3的目的是调节pH,使溶液中的
(2)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)
2+ 4 |
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO
- 3 |
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液.

 [Fe2(OH)4]2++2H+
[Fe2(OH)4]2++2H+

