题目内容
在273K、1.01×105Pa条件下,将1.40g氮气、1.60g氧气和4.00g氩气混合.该混合气体的体积是( )
| A、3.36L |
| B、6.72 L |
| C、8.96 L |
| D、4.48 L |
考点:气体摩尔体积
专题:
分析:根据n=
=
计算.
| m |
| M |
| V |
| Vm |
解答:
解:n(N2)=
=0.05mol;
n(O2)=
=0.05mol;
n(Ar)=
=0.1mol,
气体的总物质的量为0.2mol,则总体积为0.2mol×22.4L/mol=4.48L.
故选:D.
| 1.40g |
| 28g/mol |
n(O2)=
| 1.60g |
| 32g/mol |
n(Ar)=
| 4.00g |
| 40g/mol |
气体的总物质的量为0.2mol,则总体积为0.2mol×22.4L/mol=4.48L.
故选:D.
点评:本题考查物质的量的有关计算,为高频考点,比较基础,注意对公式的理解掌握,注意气体摩尔体积的使用条件与对象.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用H2O2和H2SO4的混合溶液可溶解废旧印刷电路板上的铜.已知:Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64.39kJ?mol -11H2O2(l)═2H2O(l)+O2(g)△H=-196.46kJ?mol -1H2(g)+
O2(g)═H2O(l))△H=-285.84kJ?mol -1在H2SO4溶液中,Cu与H2O2反应生成Cu2+(aq)和H2O(l)的反应热△H等于( )
| 1 |
| 2 |
| A、-417.91kJ?mol -1 |
| B、-319.68kJ?mol -1 |
| C、+546.69kJ?mol -1 |
| D、-448.46kJ?mol -1 |
关甲烷的图示中不能反映甲烷分子为立体结构的是( )
A、结构式: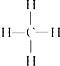 |
B、球棍模型: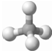 |
C、比例模型: |
D、分子结构示意图: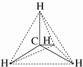 |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、1molFeCl3完全水解生成1molFe(OH)3胶粒 |
| B、常温常压下,1NA个一氯甲烷分子的体积大于22.4L |
| C、T℃时,1 L pH=6纯水中,含10-8NA个OH- |
| D、3.4g NH3中含N-H键数目为0.2NA |
热还原法冶炼金属的反应一定是( )
| A、置换反应 | B、分解反应 |
| C、复分解反应 | D、氧化还原反应 |
下列化学用语或说法正确的是( )
| A、向含有1 mol KAl(SO4)2的溶液中加入Ba(OH)2溶液至沉淀质量最大时,沉淀的总的物质的量为2.5 mol |
| B、FeCl2、Fe(OH)3均可通过化合反应制得 |
| C、由水电离的c(H+)为10-13mol/L的溶液,Na+、NO3-、SO42-、I-一定能大量共存 |
| D、可以用浓盐酸酸化的KMnO4溶液与H2O2混合,以证明H2O2具有还原性:2MnO4-+8H++5H2O2=2Mn2++5O2↑+8H2O |
下列反应中,有沉淀产生且不会消失的是( )
| A、将CO2通入澄清石灰水溶液中,直至过量 |
| B、将NaOH溶液逐滴滴入AlCl3溶液中,直至过量 |
| C、向AlCl3溶液中逐滴滴入稀硫酸 |
| D、向NaOH溶液中逐滴滴入Fe2(SO4)3溶液直至过量 |