题目内容
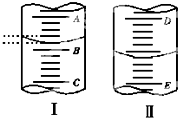 (1)图Ⅰ表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量简中液体的体积是 mL.
(1)图Ⅰ表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量简中液体的体积是 mL.(2)图Ⅱ表示50mL滴定管中液画的位置,如果液面处的读数是a,则滴定管中液体的体积 (填代号).( )
分析:(1)用量筒读数时,注意它的刻度值从下到上逐渐增大,根据图Ⅰ根据刻度A为4,则B刻度为3,再根据每个小刻度为0.2mL计算出量筒中的液体;
(2)根据滴定管刻度值从上到下刻度逐渐增大以及测量原理,注意滴定管最大刻度下方无刻度.
(2)根据滴定管刻度值从上到下刻度逐渐增大以及测量原理,注意滴定管最大刻度下方无刻度.
解答:解:(1)由图知量筒A与B之间有五个小格,所以一个小格代表0.2ml,即此量筒的分度值为0.2ml,如果刻度A为4,则刻度B为3,凹液面最低处与3mL以上一个刻度处相平,所以液体体积为3.2mL,
(2)滴定管刻度值从上到下刻度逐渐增大,由于滴定管最大刻度下方无刻度,50mL滴定管中实际盛放液体的体积大于50ml,如果液面处的读数是a,则滴定管中液体的体积大于(50-a)ml,
故选:D.
(2)滴定管刻度值从上到下刻度逐渐增大,由于滴定管最大刻度下方无刻度,50mL滴定管中实际盛放液体的体积大于50ml,如果液面处的读数是a,则滴定管中液体的体积大于(50-a)ml,
故选:D.
点评:本题考查了计量仪器的构造及其使用方法,题目难度不大,注意量筒刻度值从下到上逐渐增大,而滴定管刻度值从上到下刻度逐渐增大,且最大刻度下方无刻度.

练习册系列答案
相关题目
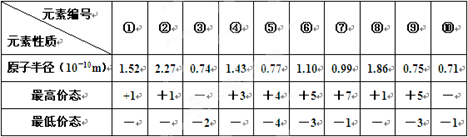
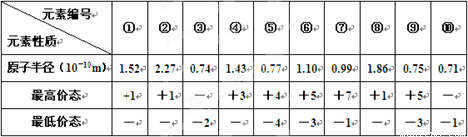
下表列出了前20号元素中的某些元素性质的有关数据:试回答下列问题:
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
| 原子半径(10—10m) | 1.5 | 2.2 | 0.7 | 1.4 | 0.7 | 1.1 | 0.9 | 1.8 | 0.7 | 0.7 |
| 最高价态 | +1 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | — |
| 最低价态 | — | — | -2 | — | -4 | -3 | -1 | — | -3 | -1 |
(1)以上10种元素的原子中,最容易失电子的是 (填写元素符号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是 、 (写分子式)。某元素R的原子半径为1.02×10—10m,该元素在周期表中的位置是 ;若物质Na2R2是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式 。
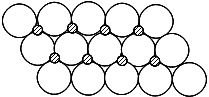
(3)元素⑤的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的②单质相互作用,形成某种青铜色的物质(其中“●”表示元素②的原子),右图为该物质部分原子分布示意图,请根据图找出原子排列规律并写出该物质的化学式 。

 02×10-10m,该元素在周期表中位于 ;若物质Na2R3是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式 。
02×10-10m,该元素在周期表中位于 ;若物质Na2R3是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式 。