题目内容
8.A、B、C、X均为常见的纯净物,它们之间有如下转化关系(副产品已略去).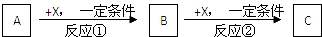
试回答:
(1)若X是强氧化性单质,则A不可能是de.
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为FeCl3;
(3)若A、B、C为含某金属元素的无机化合物,X为强电解质,焰色反应为黄色,A溶液与C溶液反应生成B,则B的化学式为Al(OH)3,X的化学式NaOH,反应①的离子方程式为Al3++3OH-═Al(OH)3↓.
分析 (1)若X是强氧化性单质,由转化关系可知,A、B、C中含有的相同元素必须是变价元素,结合选项中物质的性质分析解答;
(2)若X是金属单质,由转化关系可知,X为变价金属,A为强氧化性物质,向C的水溶液中滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则C中含有氯离子,则X为Fe,A为Cl2,B为FeCl3,C为FeCl2;
(3)若A、B、C为含某金属元素的无机化合物,且A+C→B,考虑Al的化合物的相互转化,X为强电解质,焰色反应为黄色,则A为铝盐,X为NaOH,B为Al(OH)3,C为NaAlO2.
解答 解:(1)若X是强氧化性单质,由转化关系,可知A、B、C中含有的相同元素必须是变价元素,
a.S和氧气反应生成二氧化硫,二氧化硫和氧气反应生成三氧化硫,符合转化关系,故不选;
b.N2 和氧气反应生成一氧化氮,一氧化氮和氧气反应生成二氧化氮,符合转化关系,故不选;
c.Na和氧气反应生成氧化钠,氧化钠和氧气反应生成过氧化钠,符合转化关系,故不选;
d.Mg和氧气反应生成氧化镁,氧化镁和氧气不反应,所以不符合转化关系,故选;
e.Al和氧气反应生成氧化铝,氧化铝和氧气不反应,所以不符合转化关系,故选;
故答案为:de;
(2)若X是金属单质,由转化关系可知,X为变价金属,A为强氧化性物质,向C的水溶液中滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则C中含有氯离子,则X为Fe,A为Cl2,B为FeCl3,C为FeCl2,
故答案为:FeCl3;
(3)若A、B、C为含某金属元素的无机化合物,且A+C→B,考虑Al的化合物的相互转化,X为强电解质,焰色反应为黄色,则A为铝盐,X为NaOH,B为Al(OH)3,C为NaAlO2,反应①的离子方程式为:Al3++3OH-═Al(OH)3↓,
故答案为:Al(OH)3;NaOH;Al3++3OH-═Al(OH)3↓.
点评 本题考查无机物推断,基本属于开放性题目,旨在考查学生对元素化合物知识的熟练掌握程度,注意掌握中学常见连续反应.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 1.8g NH4+含有的电子数为0.1NA | |
| B. | 2.3g金属钠反应生成Na2O2时失去的电子数为0.2NA | |
| C. | 标准状况下,11.2L的CCl4所含的分子数为0.5NA | |
| D. | 24.0g O2分子和24g O3分子所含的氧原子数目相等 |
| A. | ③①②④ | B. | ①②③④ | C. | ③①④② | D. | ①④③② |
| A. | NH4+、Ag+、NO3-、MnO4 - | B. | Fe3+、Fe2+、SO42-、Cl- | ||
| C. | K+、Na+、AlO2-、CO32- | D. | Al3+、Mg2+、SO42-、NO3- |
| A. | 2C2H6(g)+7O2(g)═4CO2(g)+6H2O(l)△H=-3 119.6 kJ•mol-1 | |
| B. | C2H6(g)+$\frac{5}{2}$O2(g)═2CO(g)+3H2O(g)△H=-1 559.8 kJ•mol-1 | |
| C. | C2H6(g)+$\frac{7}{2}$O2(g)═2CO2(g)+3H2O(g)△H=-1 559.8 kJ•mol-1 | |
| D. | C2H6(g)+$\frac{7}{2}$O2(g)═2CO2(g)+3H2O(l)△H=-1 559.8 kJ•mol-1 |
| A. | 若Z(OH)n为强碱,则W(OH)m也一定为强碱 | |
| B. | 若HnXOm为强酸,则Z的气态氢化物溶于水一定显酸性 | |
| C. | Z可以从W的盐溶液中将W置换出来 | |
| D. | 若Z的最高正价为+3价,则W的氢化物水溶液一定显碱性 |
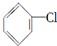 制取
制取 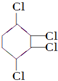 ,其合成流程如下:
,其合成流程如下: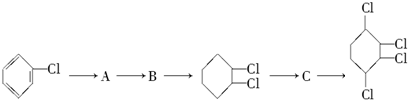
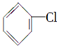 到A的转化是与氢气在催化剂存在条件下的加成反应,请从左向右依次填写其余每步反应所属的类型是b、c、b、c、b.
到A的转化是与氢气在催化剂存在条件下的加成反应,请从左向右依次填写其余每步反应所属的类型是b、c、b、c、b.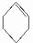 .
.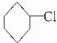 +NaOH$→_{△}^{乙醇}$
+NaOH$→_{△}^{乙醇}$