题目内容
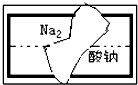 某中学学习小组在帮助老师整理实验室的化学试剂时,发现一盛有白色固体的试剂瓶,标签破损(如图),请你根据已掌握的知识,对该药品可能是什么物质作出猜想(4种),并设计实验验证.
某中学学习小组在帮助老师整理实验室的化学试剂时,发现一盛有白色固体的试剂瓶,标签破损(如图),请你根据已掌握的知识,对该药品可能是什么物质作出猜想(4种),并设计实验验证.(1)猜想:这种试剂可能是
(2)实验验证:
考点:物质的检验和鉴别的实验方案设计
专题:物质检验鉴别题
分析:结合图可知,可能为硫酸钠、碳酸钠、亚硫酸钠等,检验硫酸根离子利用盐酸和氯化钡,检验碳酸根离子,利用盐酸、品红及石灰水,检验亚硫酸根离子利用盐酸和品红,以此来解答.
解答:
解:结合图可知,可能为硫酸钠、碳酸钠、亚硫酸钠、硅酸钠等,
若为Na2SO4,需要试剂为稀盐酸和BaCl2溶液,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入BaCl2溶液,如果生成白色沉淀,则原溶液是Na2SO4溶液;
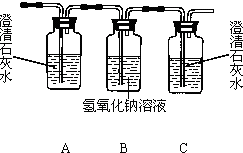
若为Na2CO3,需要试剂为稀盐酸、品红试纸和澄清石灰水,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若产生的无色气体不能使湿润的品红试纸变红,但能使澄清石灰水变浑浊.原溶液是Na2CO3溶液;
若为Na2SO3,需要试剂为稀盐酸、品红试纸,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若产生的无色气体能使湿润的品红试纸变红,原溶液是Na2SO3溶液;
若为Na2SiO3,需要实际为稀盐酸,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若产生白色沉淀,则原溶液是Na2SiO3溶液,
故答案为:硫酸钠、碳酸钠、亚硫酸钠、硅酸钠;
若为Na2SO4,需要试剂为稀盐酸和BaCl2溶液,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入BaCl2溶液,如果生成白色沉淀,则原溶液是Na2SO4溶液;
若为Na2CO3,需要试剂为稀盐酸、品红试纸和澄清石灰水,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若产生的无色气体不能使湿润的品红试纸变红,但能使澄清石灰水变浑浊.原溶液是Na2CO3溶液;
若为Na2SO3,需要试剂为稀盐酸、品红试纸,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若产生的无色气体能使湿润的品红试纸变红,原溶液是Na2SO3溶液;
若为Na2SiO3,需要实际为稀盐酸,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若产生白色沉淀,则原溶液是Na2SiO3溶液,
故答案为:硫酸钠、碳酸钠、亚硫酸钠、硅酸钠;
| 猜想的化学物质 | 检验需要的试剂 | 操作、现象和结论 | |
| 1 | Na2SO4 | 稀盐酸和BaCl2溶液 | 取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入BaCl2溶液,如果生成白色沉淀,则原溶液是Na2SO4溶液 |
| 2 | Na2CO3 | 稀盐酸、品红试纸和澄清石灰水 | 取少量该溶液于试管中,滴入稀盐酸,若产生的无色气体不能使湿润的品红试纸变红,但能使澄清石灰水变浑浊.原溶液是Na2CO3溶液. |
| 3 | Na2SO3 | 稀盐酸、品红试纸 | 取少量该溶液于试管中,滴入稀盐酸,若产生的无色气体能使湿润的品红试纸变红,原溶液是Na2SO3溶液. |
| 4 | Na2SiO3 | 稀盐酸 | 取少量该溶液于试管中,滴入稀盐酸,若产生白色沉淀,则原溶液是Na2SiO3溶液. |
点评:本题考查物质鉴别和检验方法的选择和应用,为高频考点,侧重钠盐及阴离子检验的考查,注意试剂的选择、现象与结论的关系即可解答,具有一定的开放性,题目难度不大,注意Na2S、Na2S2O3不常见.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
有关物质与反应分类的下列说法中,正确的是( )
| A、硅酸钠是钠盐,也是硅酸盐 |
| B、碳酸钠使无色酚酞试液变红,属于碱 |
| C、CO2溶于水能导电,属电解质 |
| D、CO还原氧化铁获得铁,属于置换反应 |
下列试剂的保存方法正确的是( )
| A、氢氟酸存放在玻璃瓶中 |
| B、烧碱溶液存放在带橡皮塞的玻璃瓶中 |
| C、水玻璃存放在滴瓶中 |
| D、金属钠保存在冷水里 |
工业废水中常含有Cu2+、Cd2+、Pb2+等重金属离子,可通过加入过量的难溶电解质 FeS、MnS,使这些金属离子形成硫化物沉淀除去.根据以上事实,可推知FeS、MnS具有的相关性质是( )
| A、在水中的溶解能力大于CuS、CdS、PbS |
| B、在水中的溶解能力小于CuS、CdS、PbS |
| C、在水中的溶解能力与CuS、CdS、PbS相同 |
| D、二者均具有较强的吸附性 |