题目内容
密闭容器中的可逆反应 2HI(g)?I2(g)+H2(g),能说明反应达到平衡的是( )
| A、容器内压强不变 |
| B、单位时间内消耗2molHI,同时生成1molH2 |
| C、HI的浓度与I2的浓度相等 |
| D、混合气体的颜色不变 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论.
解答:
解:A.反应前后气体的体积不变,故容器总压强不随时间改变不能作为判断是否达到化学平衡状态的依据,故A错误;
B.单位时间内消耗2molHI是正反应,同时生成1molH2也为正反应,故B错误;
C.平衡时各物质的浓度取决于物质的起始物质的量和转化率,故HI的浓度与I2的浓度相等不能作为判断是否达到平衡状态的依据,故C错误,
D.HI和氢气为无色气体,碘蒸气为紫红色气体,故混合气体的颜色不变可作为判断是否达到平衡状态的依据,故D正确,
故选D.
B.单位时间内消耗2molHI是正反应,同时生成1molH2也为正反应,故B错误;
C.平衡时各物质的浓度取决于物质的起始物质的量和转化率,故HI的浓度与I2的浓度相等不能作为判断是否达到平衡状态的依据,故C错误,
D.HI和氢气为无色气体,碘蒸气为紫红色气体,故混合气体的颜色不变可作为判断是否达到平衡状态的依据,故D正确,
故选D.
点评:本题考查化学平衡状态的判断,题目难度不大.要注意把握平衡状态的特征.

练习册系列答案
相关题目
下列说法正确的是( )
| A、元素铯的两种核素137Cs比133Cs多四个质子 |
| B、等质量的H2、D2、T2三种气体的电子数之比为2:3:6 |
| C、一种元素只能有一种质量数 |
| D、在氮原子中,质子数为7而中子数不一定为7 |
在电解水制取H2和O2时,为了增强导电性,常常要加入一些电解质,最好选用( )
| A、NaCl |
| B、HC1 |
| C、NaOH |
| D、CuSO4 |
有机化学中取代反应范畴很广,下列反应不属于取代反应的是( )
A、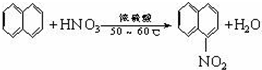 |
B、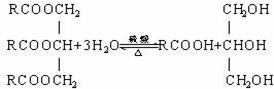 |
C、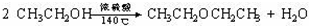 |
D、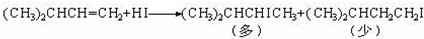 |
根据所学知识,下列离子在溶液中易与SCN-结合的是( )
| A、K+ | ||
B、NH
| ||
| C、Na+ | ||
| D、Fe3+ |
可逆反应2NO2
2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
| △ |
| A、NO2、NO和O2三者共存 |
| B、单位时间内生成n molO2的同时生成2n mol NO |
| C、容器中颜色不再变化 |
| D、容器中NO2、NO、O2的物质的量浓度之比为2:2:1的状态 |
反应:4A(g)+5B(g)=4C(g)+6D(g)在不同条件下进行,用不同的物质表示其反应速率如下,则此反应在不同条件下进行最快的是( )
| A、v(A)=2 mol?L-1?min-1 |
| B、v(B)=3 mol?L-1?min-1 |
| C、v(C)=1 mol?L-1?min-1 |
| D、v(D)=2.4 mol?L-1?min-1 |
下列各组物质中,化学键类型相同,晶体类型也相同的是( )
| A、CH4和H2O |
| B、KCl和HCl |
| C、Cl2和KCl |
| D、SiO2和CO2 |
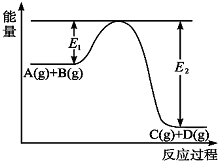 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.