题目内容
写出下列反应的化学方程式,并注明的反应类型
(1)由乙烯制备聚乙烯的反应
(2)用甲苯制TNT的反应
(3)溴乙烷与NaOH的乙醇溶液共热 .
(1)由乙烯制备聚乙烯的反应
(2)用甲苯制TNT的反应
(3)溴乙烷与NaOH的乙醇溶液共热
考点:有机物的结构和性质
专题:有机反应
分析:(1)乙烯含有碳碳双键,可发生加聚反应生成聚乙烯;
(2)甲苯与浓硝酸发生取代反应可生成TNT,即三硝基甲苯;
(3)溴乙烷与NaOH的乙醇溶液共热,发生消去反应生成乙烯.
(2)甲苯与浓硝酸发生取代反应可生成TNT,即三硝基甲苯;
(3)溴乙烷与NaOH的乙醇溶液共热,发生消去反应生成乙烯.
解答:
解:(1)乙烯含有碳碳双键,可发生加聚反应生成聚乙烯,方程式为nCH2=CH2
 ,
,
故答案为:nCH2=CH2
 ,加聚反应(或聚合反应);
,加聚反应(或聚合反应);
(2)甲苯与浓硝酸发生取代反应可生成TNT,即三硝基甲苯,反应的化学方程式为 ,
,
故答案为: ,取代反应;
,取代反应;
(3)溴乙烷与NaOH的乙醇溶液共热,发生消去反应生成乙烯,溴乙烷与氢氧化钠乙醇溶液加热反应方程式:CH3CH2Br+NaOH
CH2=CH2↑+NaBr+H2O,
故答案为:CH3CH2Br+NaOH
CH2=CH2↑+NaBr+H2O,消去反应.
| 催化剂 |
 ,
,故答案为:nCH2=CH2
| 催化剂 |
 ,加聚反应(或聚合反应);
,加聚反应(或聚合反应);(2)甲苯与浓硝酸发生取代反应可生成TNT,即三硝基甲苯,反应的化学方程式为
 ,
,故答案为:
 ,取代反应;
,取代反应;(3)溴乙烷与NaOH的乙醇溶液共热,发生消去反应生成乙烯,溴乙烷与氢氧化钠乙醇溶液加热反应方程式:CH3CH2Br+NaOH
| 醇 |
| △ |
故答案为:CH3CH2Br+NaOH
| 醇 |
| △ |
点评:本题考查有机物的机构和性质,为高考常见题型,注意把握有机物的官能团的性质以及相关方程式的书写,为解答该题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
加入NaOH溶液后,下列溶液中的离子数目不会减少的是( )
| A、HCO3- |
| B、Fe3+ |
| C、SO42- |
| D、H+ |
关于氯化镁溶液和氢氧化铁胶体的说法中正确的是( )
| A、溶液是电中性的,胶体是带电的 |
| B、两者的分散质微粒均能透过半透膜和滤纸 |
| C、溶液中溶质分子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 |
| D、一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有 |
短周期元素A、B、C、D的原子序数依次增大,A的原子半径在所有原子中最小,B位于第VA族,A和C同主族,D原子最外层电子数与电子层数相等.下列叙述正确的是( )
| A、原子半径:C<B |
| B、元素A、C的氧化物均为共价化合物 |
| C、金属性:D>C |
| D、元素B、C、D的最高价氧化物对应水化物能相互反应 |
下列说法正确的是( )
| A、元素周期表中一共有7个周期和18个族 |
| B、金属元素的原子最外层电子数一定都小于4 |
| C、质量数相同的两种原子,一定不互为同位素 |
| D、主族元素X的原子序数为a,所在周期的元素种数为b,则与x同族的下一周期的元素Y的原于序数一定为a+b |
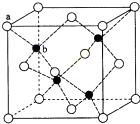 CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分.
CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分.