题目内容
25℃时,水中存在电离平衡:H2O?H++OH-△H>0.下列叙述正确的是( )
| A、升高温度,Kw增加,pH增大 |
| B、向水中加入少量NaOH固体,平衡向逆方向移动,c(OH-)增大 |
| C、向水中加入少量CH3COONa固体,平衡向正方向移动,c(H+)增大 |
| D、25℃时,纯水中c(H+)>10-7mol/L |
考点:水的电离
专题:
分析:A、温度升高,水的离子积常数增大,则pH值减小;
B、氢氧化钠溶液显碱性,纯水显中性,碱中氢氧根浓度大于水中的;
C、醋酸根水解对水的电离起到促进作用;
D、水电离出的氢离子浓度等于水电离出的氢氧根浓度,常温下等于10-7mol/L.
B、氢氧化钠溶液显碱性,纯水显中性,碱中氢氧根浓度大于水中的;
C、醋酸根水解对水的电离起到促进作用;
D、水电离出的氢离子浓度等于水电离出的氢氧根浓度,常温下等于10-7mol/L.
解答:
解:A、温度升高,水的离子积常数KW增大,则pH值减小,故A错误;
B、向水中加入氢氧化钠,溶液由中性到碱性,碱对水的电离起抑制作用,所以平衡逆向移动,c(OH-)增大,故B正确;
C、CH3COONa中的醋酸根水解对水的电离起到促进作用,电离平衡右移,c(H+)降低,故C错误;
D、水电离出的氢离子浓度等于水电离出的氢氧根浓度,常温下等于10-7mol/L,故D错误,故选B.
B、向水中加入氢氧化钠,溶液由中性到碱性,碱对水的电离起抑制作用,所以平衡逆向移动,c(OH-)增大,故B正确;
C、CH3COONa中的醋酸根水解对水的电离起到促进作用,电离平衡右移,c(H+)降低,故C错误;
D、水电离出的氢离子浓度等于水电离出的氢氧根浓度,常温下等于10-7mol/L,故D错误,故选B.
点评:本题考查学生水的电离知识,酸、碱对水的电离起抑制作用,水解的盐对水的电离起促进作用.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
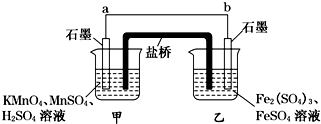
在用锌片、铜片和稀硫酸组成的原电池装置中,经过-段时间工作后,下列说法正确的是( )
| A、锌片是正极,铜片是负极 |
| B、电子是从锌片通过导线流到铜片上 |
| C、溶液中H+移向锌片被还原变成H2 |
| D、电解液的pH逐渐变小 |
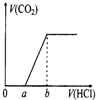 在100mL某浓度的NaOH溶液中通入一定量的CO2气体,得到溶液X,再向溶液X中逐滴加入0.1mol/L的盐酸,产生的气体体积与加入盐酸的体积关系如图所示,有关说法错误的是( )
在100mL某浓度的NaOH溶液中通入一定量的CO2气体,得到溶液X,再向溶液X中逐滴加入0.1mol/L的盐酸,产生的气体体积与加入盐酸的体积关系如图所示,有关说法错误的是( )| A、若a:b<1:2,则0~a段发生的离子反应为:CO32-+H+=HCO3- |
| B、若a:b>l:2,且b=20 mL,则原NaOH溶液的浓度为0.02 mol/L |
| C、若a:b=1:2,则溶液X中离子浓度满足:c(H+)+c(HCO3-)=c(OH-)-c(H2CO3) |
| D、a:b为任意值时,溶液X中离子浓度均满足:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) |
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )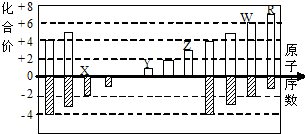

| A、原子半径:R>Y>X |
| B、气态氢化物的稳定性:R>W |
| C、WX3和水反应形成的化合物具有挥发性 |
| D、Z能和Y的最高价氧化物对应的水化物反应 |
设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、78g Na2O2与足量水充分反应时电子转移数为2NA |
| B、1 mol Na完全转化为Na2O2时,失去的电子数目为2NA |
| C、4℃、101.3kPa时,54mL H2O中含有的分子数为3NA |
| D、2L1mol/L Na2SO4溶液中离子总数为3NA |