题目内容
3.设NA为阿伏加德罗常数的值,下列说法中正确的是( )| A. | 标准状况下,22.4 L甲苯所含的分子数约为NA | |
| B. | 室温下,2.8g乙烯与丙烯的混合物中含碳原子的数目为0.2NA | |
| C. | 1 mol C30H62分子中含有共价键的数目为92NA | |
| D. | 1 mol氯气和足量甲烷在光照条件下反应可生成2NA个氯化氢分子 |
分析 A.甲苯标准状况下不是气体;
B.乙烯与丙烯最简式为CH2,计算2.8gCH2中所含碳原子即可;
C.通式判断有机物为烷烃CnH2n+2结构,依据烷烃分子结构计算化学键,化学键为n-1+2n+2=3n+1;
D.取代反应是有出又进,1mol氯气分子取代1mol氢原子,同时生成1molHCl;
解答 解:A.标准状况下,甲苯不是气体,22.4 L甲苯物质的量不是1mol,故A错误;
B.乙烯与丙烯最简式为CH2,计算2.8gCH2中所含碳原子,2.8g乙烯与丙烯的混合物中含碳原子的数目=$\frac{2.8g}{14g/mol}$×1×NA=0.2NA ,故B正确;
C.1 mol C30H62分子中含有共价键的数目=(30-1+62)×NA=91NA ,故C错误;
D.取代反应是有出又进,1mol氯气分子取代1mol氢原子,1 mol氯气和足量甲烷在光照条件下反应可生成NA个氯化氢分子,故D错误;
故选B.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件应用、物质结构、取代反应的特征等知识点,掌握基础是解题关键,题目难度中等.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案
相关题目
14.下列说法正确的是( )
| A. | 化学式符合Cn(H2O)m组成的一定是糖 | B. | 糖类物质都不能水解 | ||
| C. | 自然界中无单糖 | D. | 糖类物质是人类最基本的能量来源 |
11.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 标准状态下,22.4L氯化氢中含有氯原子的数目为NA | |
| B. | 常温常压下,7.0g乙烯与丙稀的混合物中含有碳原子的数目为NA | |
| C. | 50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA | |
| D. | 某密闭容器盛有0.1mol N2和0.3mol H2,在一定条件下充分反应,转移电子的数目为0.6NA |
8.将1L 0.1mol/L BaCl2溶液与足量稀硫酸充分反应放出a kJ热量;将1L 0.5mol/LHCl溶液与足量CH3COONa溶液充分反应放出b kJ热量(不考虑醋酸钠水解);将0.5L1mol/L H2SO4溶液与足量(CH3COO)2Ba(可溶性强电解质)溶液反应放出的热量为( )
| A. | (5a+2b) kJ | B. | (4b-10a) kJ | C. | (5a-2b) kJ | D. | (10a+4b) kJ |
15.下列化学用语的书写,正确的是( )
| A. | 氯气的分子式 Cl | B. | 钠原子的结构示意图 | ||
| C. | N2的电子式:N:::N: | D. | HClO的结构式 H-Cl-O |
12.在下列实验中,应将温度计插入水浴中的是( )
| A. | 乙醛的银镜反应 | B. | 由苯制硝基苯 | ||
| C. | 由酒精制乙烯 | D. | 由乙酸与乙醇反应制乙酸乙酯 |
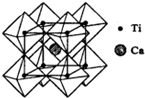 钛被称为继铁、铝之后的第三金属,制备金属钛的一种流程如下:
钛被称为继铁、铝之后的第三金属,制备金属钛的一种流程如下: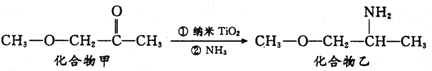
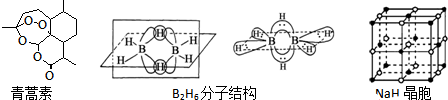
 ;
;