题目内容
向50mL稀硫酸和稀盐酸的混合溶液中,加入3.42g氢氧化钡粉末,充分反应后过滤,得干燥沉淀物1.165g,所得溶液的氢氧根离子浓度为0.2mol/L,试求原混合溶液中SO42-和Cl-的物质的量(假定在混合液中加入氢氧化钡粉末后体积未变).
考点:有关混合物反应的计算
专题:计算题
分析:n(Ba(OH)2)=
=0.02mol,硫酸根离子和钡离子反应生成硫酸钡沉淀,n(BaSO4)=
=0.005mol<0.02mol,则钡离子有剩余,根据n(BaSO4)计算溶液中n(SO42- );
氢氧化钡中n(OH-)=2n(Ba(OH)2)=0.04mol,溶液中n(OH-)=0.2mol/L×0.05L=0.01mol,参加反应的n(OH-)=0.04mol-0.01mol=0.03mol,氢离子和氢氧根离子以1:1反应,所以参加反应的n(H+)=n(OH-)=0.03mol,再结合电荷守恒计算n(Cl-).
| 3.42g |
| 171g/mol |
| 1.165g |
| 233g/mol |
氢氧化钡中n(OH-)=2n(Ba(OH)2)=0.04mol,溶液中n(OH-)=0.2mol/L×0.05L=0.01mol,参加反应的n(OH-)=0.04mol-0.01mol=0.03mol,氢离子和氢氧根离子以1:1反应,所以参加反应的n(H+)=n(OH-)=0.03mol,再结合电荷守恒计算n(Cl-).
解答:
解:n(Ba(OH)2)=
=0.02mol,硫酸根离子和钡离子反应生成硫酸钡沉淀,n(BaSO4)=
=0.005mol<0.02mol,则钡离子有剩余,则n(BaSO4)=n(SO42- )=0.005mol;
氢氧化钡中n(OH-)=2n(Ba(OH)2)=0.04mol,溶液中n(OH-)=0.2mol/L×0.05L=0.01mol,参加反应的n(OH-)=0.04mol-0.01mol=0.03mol,氢离子和氢氧根离子以1:1反应,所以参加反应的n(H+)=n(OH-)=0.03mol,硫酸和盐酸混合溶液中存在结合电荷守恒,所以得2n(SO42- )+n(Cl-)=n(H+),n(Cl-)=n(H+)-2n(SO42- )=0.03mol-2×0.005mol=0.02mol,
答:原溶液中SO42-和Cl-的物质的量分别是0.005mol、0.02mol.
| 3.42g |
| 171g/mol |
| 1.165g |
| 233g/mol |
氢氧化钡中n(OH-)=2n(Ba(OH)2)=0.04mol,溶液中n(OH-)=0.2mol/L×0.05L=0.01mol,参加反应的n(OH-)=0.04mol-0.01mol=0.03mol,氢离子和氢氧根离子以1:1反应,所以参加反应的n(H+)=n(OH-)=0.03mol,硫酸和盐酸混合溶液中存在结合电荷守恒,所以得2n(SO42- )+n(Cl-)=n(H+),n(Cl-)=n(H+)-2n(SO42- )=0.03mol-2×0.005mol=0.02mol,
答:原溶液中SO42-和Cl-的物质的量分别是0.005mol、0.02mol.
点评:本题考查了混合物的计算,题目难度中等,注意计算过程中原子守恒、电荷守恒的应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
| A、经测定某物质只含一种元素,则该物质一定是单质 |
| B、难溶于水的电解质一定是弱电解质 |
| C、离子化合物中可能含有共价键 |
| D、既能与酸又能与碱反应的化合物一定是两性化合物 |
下列书写正确的是( )
| A、硫化钠水解:S2-+2H2O?H2S+2OH- |
| B、碳酸钠与醋酸溶液反应:CO32-+2H+=H2O+CO2↑ |
| C、HCO3-的电离:H2O+HCO3-?CO32-+H3O+ |
| D、NaHS在水中的电离:NaHS?Na++HS- HS-?H++S2- |
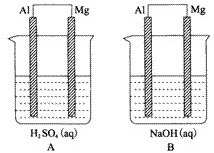
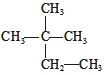 ③白磷 ④氯水 ⑤
③白磷 ④氯水 ⑤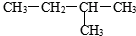 ⑥
⑥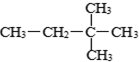 ⑧2,2-二甲基丁烷⑨红磷 ⑩
⑧2,2-二甲基丁烷⑨红磷 ⑩ 如图所示,水槽中试管内有一枚铁钉,放置数天观察:
如图所示,水槽中试管内有一枚铁钉,放置数天观察:
 某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g)△H>0.在三种不同条件下进行,其中NO、O2的起始浓度都为0mol?L-1,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol?L-1)随时间(min)的变化如图所示.
某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g)△H>0.在三种不同条件下进行,其中NO、O2的起始浓度都为0mol?L-1,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol?L-1)随时间(min)的变化如图所示.