题目内容
A、B、C三种无色可溶性电解质分别是由Na+、Ag+、Ba2+、OH-、NO3-、CO32-中不同的阴、阳离子所组成.经实验A溶液、B溶液、C溶液均可与盐酸反应,其中A产生白色沉淀,B产生气泡,C无明显现象.则A为 ;B为 ;C为 (填化学式).
写出A与盐酸反应的离子方程式 ;
写出B与盐酸反应的离子方程式 ;
写出C与H2SO4反应的离子方程式 .
写出A与盐酸反应的离子方程式
写出B与盐酸反应的离子方程式
写出C与H2SO4反应的离子方程式
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:先根据离子共存判断离子之间的组合:Ag+只能结合NO3-形成硝酸银、剩下的离子中Ba2+只能结合OH-形成氢氧化钡、最后的离子结合形成碳酸钠,然后根据A、B能够与盐酸反应的现象判断A、B组成,从而明确A、B、C的名称.
解答:
解:A、B、C为三种无色可溶盐,则Ag+只能结合NO3-形成AgNO3、剩下的离子中Ba2+只能结合OH-形成Ba(OH)2,另一种物质则为Na2CO3;
A溶液、B溶液均可与盐酸反应,其中A产生白色沉淀,则A为AgNO3;B与盐酸产生气泡,所以B为Na2CO3,C无明显现象,则C为Ba(OH)2,硝酸银与盐酸反应生成氯化银沉淀,化学反应方程式为:Ag++Cl-=AgCl↓;Na2CO3与盐酸反应生成二氧化碳、氯化钠和水,故离子反应方程式为:CO32-+2H+=CO2↑+H2O;氢氧化钡与硫酸反应生成硫酸钡和水,故离子反应方程式为:Ba2++2OH-+2H++SO 42-=BaSO4↓+2H2O,
故答案为:AgNO3;Na2CO3;BaCl2;Ag++Cl-=AgCl↓;CO32-+2H+=CO2↑+H2O;Ba2++2OH-+2H++SO 42-=BaSO4↓+2H2O.
A溶液、B溶液均可与盐酸反应,其中A产生白色沉淀,则A为AgNO3;B与盐酸产生气泡,所以B为Na2CO3,C无明显现象,则C为Ba(OH)2,硝酸银与盐酸反应生成氯化银沉淀,化学反应方程式为:Ag++Cl-=AgCl↓;Na2CO3与盐酸反应生成二氧化碳、氯化钠和水,故离子反应方程式为:CO32-+2H+=CO2↑+H2O;氢氧化钡与硫酸反应生成硫酸钡和水,故离子反应方程式为:Ba2++2OH-+2H++SO 42-=BaSO4↓+2H2O,
故答案为:AgNO3;Na2CO3;BaCl2;Ag++Cl-=AgCl↓;CO32-+2H+=CO2↑+H2O;Ba2++2OH-+2H++SO 42-=BaSO4↓+2H2O.
点评:本题考查了未知物的检验,离子反应方程式的书写,题目难度不大,注意掌握常见物质的检验方法,明确常见物质的性质及反应现象是解答本题的关键,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
在200mL某硫酸盐溶液中,含有1.5NA个SO42-,(NA表示阿佛加德罗常数的值)同时含有NA个金属离子,则该硫酸盐的物质的量浓度为( )
| A、1mol/L |
| B、2.5mol/L |
| C、5mol/L |
| D、2mol/L |
0.5L AlCl3溶液中Cl-为1.5mol.则AlCl3溶液的物质的量浓度为( )
| A、0.1 mol?L-1 |
| B、1 mol?L-1 |
| C、3 mol?L-1 |
| D、1.5 mol?L-1 |
下列各组离子在指定溶液中,可能大量共存的是( )
| A、酸性溶液中:Fe2+、Ag+、NO3-、I- |
| B、pH=1的溶液中:Na+、[Al(OH)4]-、K+、SO32- |
| C、加入Al能放出H2的溶液中:Mg2+、NH4+、Cl-、SO42- |
| D、水电离的c(H+)=10-12mol?L-1的溶液中:Cl-、HCO3-、NH4+、SO32- |
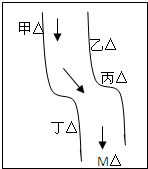 在一条鱼、虾绝迹的小河边有四座工厂:甲、乙、丙、丁(如图所示),它们排出的废液里,每个工厂只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某中学环保小组对河水检测时发现:①甲处河水呈乳白色,②乙处河水呈红褐色,③丙处河水由浑变清,④丁处产生气泡,河水仍清,⑤M处水样的pH小于7.请判断:
在一条鱼、虾绝迹的小河边有四座工厂:甲、乙、丙、丁(如图所示),它们排出的废液里,每个工厂只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某中学环保小组对河水检测时发现:①甲处河水呈乳白色,②乙处河水呈红褐色,③丙处河水由浑变清,④丁处产生气泡,河水仍清,⑤M处水样的pH小于7.请判断: