题目内容
6.下列说法正确的是( )| A. | 在常温、常压下11.2L N2含有的分子数为0.5NA | |
| B. | 标况下,22.4LH2的分子数为NA | |
| C. | 标况下,18g水的体积是22.4L | |
| D. | 1molSO2的体积是22.4L |
分析 A、不是标准状况下,不能使用标况下的气体摩尔体积计算氮气的物质的量;
B、标况下22.4LH2的物质的量为1mol;
C、水是液体,而气体摩尔体积只适用于气体;
D、状况不知,气体摩尔体积不知.
解答 解:A、常温常压下,不能使用标况下的气体摩尔体积计算氮气的物质的量及分子数,故A错误;
B、标况下22.4LH2的物质的量为1mol,所以分子数为NA,故B正确;
C、水是液体,而气体摩尔体积只适用于气体,故C错误;
D、状况不知,气体摩尔体积不知,故D错误;
故选B.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意标况下气体摩尔体积的使用条件,阿伏加德罗常数是高考的“热点”,它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容.

练习册系列答案
相关题目
17.下列化合物,不能通过化合反应得到的是( )
| A. | Al(OH)3 | B. | AlCl3 | C. | Fe(OH)3 | D. | FeCl2 |
14.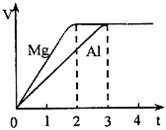 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )
 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图,下列说法正确的是( )| A. | 反应消耗镁、铝的物质的量之比是3:2 | |
| B. | 反应消耗镁、铝的质量之比是3:2 | |
| C. | 与镁和铝反应的硫酸的物质的量之比是3:2 | |
| D. | 与镁和铝反应的硫酸的质量之比是3:2 |
1.某同学用锌铜合金粉末与等体积、等浓度的稀硫酸分别做多次实验,现列出其中四组数据,请仔细阅读,回答有关问题:
(1)上表中空缺的数据应为7.25g;
(2)从上面的数据可以判断实验3(编号)是恰好完全反应.
(3)实验1中可选用硫酸锌的质量(物质名称)作为已知条件,计算放出氢气的体积是672mL(标准状况).
(4)锌铜合金中锌的质量分数为97.5%.
| 实验编号 | 锌铜合金质量/g | 硫酸/mL | 硫酸锌/g |
| 1 | 2.0 | 56 | 4.83 |
| 2 | 3.0 | 56 | |
| 3 | 4.0 | 56 | 9.66 |
| 4 | 5.0 | 56 | 9.66 |
(2)从上面的数据可以判断实验3(编号)是恰好完全反应.
(3)实验1中可选用硫酸锌的质量(物质名称)作为已知条件,计算放出氢气的体积是672mL(标准状况).
(4)锌铜合金中锌的质量分数为97.5%.
11.下列各组物质,前者属于电解质,后者属于非电解质的是( )
| A. | NaCl晶体、BaSO4 | B. | Na2SO4、酒精 | ||
| C. | 铜、二氧化硫 | D. | 熔融的KNO3、硫酸溶液 |
15.关于Na和Na+的共同点,下列叙述正确的是( )
| A. | 都显碱性 | B. | 电子层数相同 | C. | 化学性质相同 | D. | 质子数相同 |
16.电化学在日常生活中用途广泛,图甲是镁-次氯酸钠燃料电池,电池总反应为Mg+ClO-+H2O═Cl-+Mg(OH)2↓,图乙是含Cr2O72-的工业废水的处理.下列说法正确的是( )
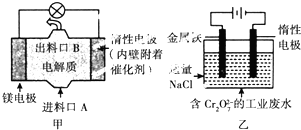

| A. | 图乙中Cr2O72-向惰性电极移动,与该极近的OH-结合转化成Cr(OH)3除去 | |
| B. | 图乙的电解池中,有0.084 g阳极材料参与反应,阴极会有336 mL的气体产生 | |
| C. | 图甲中发生的还原反应是Mg2++ClO-+H2O+2e-═Cl-+Mg(OH)2↓ | |
| D. | 若图甲中3.6 g镁溶液产生的电量用以图乙废水处理,理论可产生10.7 g氢氧化铁沉淀 |