题目内容
Ⅰ.北京时间11月1日清晨5时58分07秒,中国“长征二号F”遥八运载火箭在酒泉卫星发射中心载人航天发射场点火发射,火箭的第三级使用的推进剂是液氢和液氧.
已知下面在298K时的热化学方程式:
2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ?mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890.3kJ?mol-1
C(S)+O2(g)=CO2(g);△H=-393.5kJ?mol-1
根据上面的热化学方程式完成下列问题:
(1)通过计算说明等质量的H2、C、CH4完全燃烧时放出热量最多的是 .
(2)根据以上反应,则C(S)+2H2(g)=CH4(g)的焓变△H= .
(3)已知H2O(l)=H2O(g);△H=+44.0kJ?mol-1
试写出甲烷燃烧生成二氧化碳和水蒸气时的热化学方程式: .
Ⅱ.据统计,发达国家每年由于金属腐蚀造成的直接损失约占全年国民生产总值的2%~4%,远远超出水灾、火灾、风灾、地震等自然灾害造成损失的总和.因此,了解金属腐蚀的原因和寻求防止金属腐蚀的方法具有重要意义.
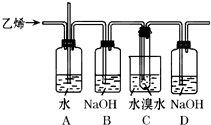
(1)分别放在如图装置(都盛有0.1mol?L-1的H2SO4溶液)中的四块相同的纯锌片,其中腐蚀最快的是 .
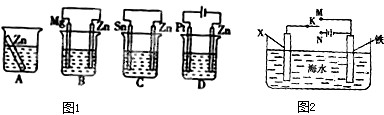
(2)利用如图装置,可以模拟铁的电化学防护.其中X为碳棒,为减缓铁的腐蚀,开关K应置于 处.若X为锌,开关K置于M处,该电化学防护法称为 .
已知下面在298K时的热化学方程式:
2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ?mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890.3kJ?mol-1
C(S)+O2(g)=CO2(g);△H=-393.5kJ?mol-1
根据上面的热化学方程式完成下列问题:
(1)通过计算说明等质量的H2、C、CH4完全燃烧时放出热量最多的是
(2)根据以上反应,则C(S)+2H2(g)=CH4(g)的焓变△H=
(3)已知H2O(l)=H2O(g);△H=+44.0kJ?mol-1
试写出甲烷燃烧生成二氧化碳和水蒸气时的热化学方程式:
Ⅱ.据统计,发达国家每年由于金属腐蚀造成的直接损失约占全年国民生产总值的2%~4%,远远超出水灾、火灾、风灾、地震等自然灾害造成损失的总和.因此,了解金属腐蚀的原因和寻求防止金属腐蚀的方法具有重要意义.
(1)分别放在如图装置(都盛有0.1mol?L-1的H2SO4溶液)中的四块相同的纯锌片,其中腐蚀最快的是

(2)利用如图装置,可以模拟铁的电化学防护.其中X为碳棒,为减缓铁的腐蚀,开关K应置于
考点:热化学方程式,金属的电化学腐蚀与防护
专题:化学反应中的能量变化,电化学专题
分析:Ⅰ、(1)根据热化学方程式的含义进行计算;
(2)根据盖斯定律来计算化学反应的焓变;
(3)根据盖斯定律来解答;
Ⅱ、(1)金属腐蚀快慢顺序是:电解池阳极>原电池负极>化学腐蚀>原电池正极>电解池阴极;
(2)作原电池正极或作电解池阴极的金属被保护.
(2)根据盖斯定律来计算化学反应的焓变;
(3)根据盖斯定律来解答;
Ⅱ、(1)金属腐蚀快慢顺序是:电解池阳极>原电池负极>化学腐蚀>原电池正极>电解池阴极;
(2)作原电池正极或作电解池阴极的金属被保护.
解答:
解:Ⅰ、(1)设质量都为m,相同质量的H2、CH4、C完全燃烧时,放出热量分别是
×m、
×m、
×m、最大值应为
×m,因此相同质量的H2、CH4、C完全燃烧时,放出热量最多的是H2,
故答案为:H2;
(2)①2H2(g)+O2(g)═2H2O(l) △H=-571.6kJ?mol-1?
②CH4(g)+2O2(g)═CO2(g)+2H2O (l) △H=-890.3kJ?mol-1?
③C(s)+O2(g)═CO2(g) △H=-393.5kJ?mol-1?
根据盖斯定律,①+③-②得热化学方程式为C(s)+2H2(g)═CH4(g)△H=-74.8 kJ?mol-1;
故答案为:-74.8 kJ?mol-1;?
(3)①CH4(g)+2O2(g)═CO2(g)+2H2O (l) △H=-890.3kJ?mol-1?
②H2O(l)═H2O(g)△H=+44.0kJ?mol-1
根据盖斯定律,①+②×2,得热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802.3 kJ?mol-1;
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802.3 kJ?mol-1;
Ⅱ、(1)金属腐蚀快慢顺序是:电解池阳极>原电池负极>化学腐蚀>原电池正极>电解池阴极,根据图知,B中锌作正极、C中锌作负极、D中锌作阴极,所以锌被腐蚀快慢顺序是:C>A>B>D,则被腐蚀最快的是C,故选C;
故答案为:C;
(2)作原电池正极或作电解池阴极的金属被保护,若X为碳棒,为减缓铁的腐蚀,则铁应作电解池阴极,所以开关K应该置于处N处;
若X为锌,开关K置于M处,该装置构成原电池,锌易失电子作负极,铁作正极而被保护,该电化学防护法称为牺牲阳极的阴极保护法,
故答案为:N;牺牲阳极的阴极保护法.
| 571.6KJ |
| 4 |
| 890.3KJ |
| 16 |
| 393.5KJ |
| 12 |
| 571.6KJ |
| 4 |
故答案为:H2;
(2)①2H2(g)+O2(g)═2H2O(l) △H=-571.6kJ?mol-1?
②CH4(g)+2O2(g)═CO2(g)+2H2O (l) △H=-890.3kJ?mol-1?
③C(s)+O2(g)═CO2(g) △H=-393.5kJ?mol-1?
根据盖斯定律,①+③-②得热化学方程式为C(s)+2H2(g)═CH4(g)△H=-74.8 kJ?mol-1;
故答案为:-74.8 kJ?mol-1;?
(3)①CH4(g)+2O2(g)═CO2(g)+2H2O (l) △H=-890.3kJ?mol-1?
②H2O(l)═H2O(g)△H=+44.0kJ?mol-1
根据盖斯定律,①+②×2,得热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802.3 kJ?mol-1;
故答案为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-802.3 kJ?mol-1;
Ⅱ、(1)金属腐蚀快慢顺序是:电解池阳极>原电池负极>化学腐蚀>原电池正极>电解池阴极,根据图知,B中锌作正极、C中锌作负极、D中锌作阴极,所以锌被腐蚀快慢顺序是:C>A>B>D,则被腐蚀最快的是C,故选C;
故答案为:C;
(2)作原电池正极或作电解池阴极的金属被保护,若X为碳棒,为减缓铁的腐蚀,则铁应作电解池阴极,所以开关K应该置于处N处;
若X为锌,开关K置于M处,该装置构成原电池,锌易失电子作负极,铁作正极而被保护,该电化学防护法称为牺牲阳极的阴极保护法,
故答案为:N;牺牲阳极的阴极保护法.
点评:本题考查了热化学方程式书写和计算应用,金属被腐蚀快慢顺序来分析,原电池、电解池原理的分析判断,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
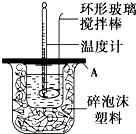 分别取40mL的0.50mol/L盐酸与0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题:
分别取40mL的0.50mol/L盐酸与0.55mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题: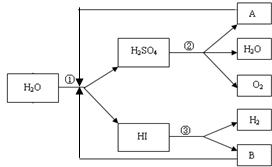 人类研究氢能源从未间断过,而热化学循环分解水制氢气是在水反应体系中加入一种中间物,经历不同的反应阶段,最终将水分解为氢气和氧气,这是一种节约能源、节省反应物料的技术,如图是一个热化学循环制氢气法的流程:
人类研究氢能源从未间断过,而热化学循环分解水制氢气是在水反应体系中加入一种中间物,经历不同的反应阶段,最终将水分解为氢气和氧气,这是一种节约能源、节省反应物料的技术,如图是一个热化学循环制氢气法的流程: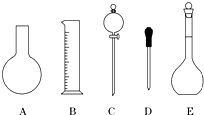 实验室用氯化钠固体配制1.00mol/L的NaCl溶液0.5L,回答下列问题
实验室用氯化钠固体配制1.00mol/L的NaCl溶液0.5L,回答下列问题
 已知1,2-二溴乙烷的主要物理性质如表:
已知1,2-二溴乙烷的主要物理性质如表:
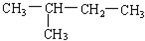 (8)
(8)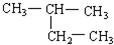 (9)新戊烷.
(9)新戊烷.