题目内容
2.下列铁的化合物不可能由化合反应直接制得的是( )| A. | FeCl2 | B. | Fe(OH)3 | C. | Fe2(SO4)3 | D. | FeCl3 |
分析 A.Fe与氯化铁反应生成氯化亚铁;
B.氢氧化亚铁、氧气、水反应生成氢氧化铁;
C.不能由化合反应生成硫酸铁;
D.Fe与氯气反应生成氯化铁.
解答 解:A.Fe与氯化铁发生化合反应直接生成氯化亚铁,故A不选;
B.氢氧化亚铁、氧气、水发生化合反应直接生成氢氧化铁,故B不选;
C.不能由化合反应生成硫酸铁,可发生复分解反应生成,故C选;
D.Fe与氯气发生化合反应直接生成氯化铁,故D不选;
故选C.
点评 本题考查金属与化合物的性质,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.认识反应条件对化学反应的影响,对学好化学具有重要意义.下列说法中正确的是( )
| A. | 偏铝酸钠溶液中加入一定量的盐酸,最终一定得到Al(OH)3沉淀 | |
| B. | 钠在敞口容器中存放或在空气中燃烧的产物都是Na2O2 | |
| C. | 向NaOH溶液中通入少量CO2或过量CO2都只生成Na2CO3 | |
| D. | 氯化铝和少量的氨水或过量的氨水反应都得到Al(OH)3沉淀 |
10.下列物质能使潮湿的有色布条褪色的是( )
| A. | HCl | B. | NaCl | C. | CO2 | D. | 干燥的氯气 |
17.《化学反应原理》选修模块从不同的视角对化学反应进行了探究分析.以下观点正确的是( )
| A. | 化学反应的反应热与反应的途径有关 | |
| B. | 电解过程中,化学能转化为电能而“储存”起来 | |
| C. | 强电解质溶液的导电能力一定强于弱电解质溶液 | |
| D. | 化学平衡常数的表达式与化学反应方程式的书写有关 |
7.下列各组离子能在溶液中大量共存的是( )
| A. | H+、Ba2+、Cl-、AlO2- | B. | Fe3+、SO42-、Na+、OH- | ||
| C. | Na+、OH-、SiO32-、Cl- | D. | Na+、HCO3-、SO42-、OH- |
14.类推的思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否,下列几种类推结论中正确的是( )
| A. | NaCl与浓H2SO4加热可制HCl,推测NaBr与浓H2SO4加热可制HBr | |
| B. | Fe与Cl2反应生成FeCl2,推测Fe与I2反应生成FeI3 | |
| C. | 不能电解AlCl3溶液来制取金属铝:推测也不能用电解MgCl2溶液来制取金属镁 | |
| D. | CO2与Na2O2反应只生成Na2O3和O2,故SO2与Na2O2反应只生成Na2SO3和O2 |
12.Na2FeO4是一种高效多功能水处理剂,应用前景十分看好.一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑.对此反应下列说法中正确的是( )
| A. | 2 mol FeSO4发生反应时,反应中共有10 mol电子转移 | |
| B. | 每生成16g氧气就有1molFe2+被还原 | |
| C. | Na2O2只作氧化剂 | |
| D. | 氧化产物只有Na2FeO4 |
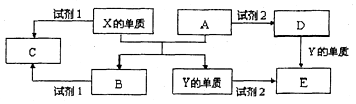 A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如图所示.
A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如图所示.