题目内容
7.火药是中国古代的四大发明之一,已知黑火药爆炸方程式为:S+2KNO3+3C═K2S+N2↑+3CO2↑,请问该反应中被硫氧化的碳和被硝酸钾氧化的碳的物质的量之比是( )| A. | 1:3 | B. | 1:4 | C. | 1:5 | D. | 1:6 |
分析 反应2KNO3+3C+S=K2S+N2↑+3CO2↑中,N、S元素化合价降低,得电子被还原,C元素化合价升高,失电子被氧化,以此解答.
解答 解:反应2KNO3+3C+S=K2S+N2↑+3CO2↑中,N、S元素化合价降低,得电子被还原,其中S元素化合价由0价降低到-2价,N元素化合价由+5价降低到0价,分别得到电子2、10个,则C该反应中被硫氧化的碳和被硝酸钾氧化的碳的物质的量之比是1:5,
故选C.
点评 本题考查氧化还原反应,侧重于学生的分析能力的考查,为高考高频考点,注意从化合价的角度分析,难度不大.

练习册系列答案
相关题目
17.下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1mol•L-1(NH4)2Fe(SO4)2溶液中;c(NH4+)+c(NH3•H2O)+c(Fe2+)=0.3mol•L-1 | |
| B. | 常温下,pH=6的NaHSO3溶液中:c(SO32-)-c(H2SO3)=9.9×10-7mol•L-1 | |
| C. | NH4HSO3溶液中滴加NaOH至溶液恰好呈中性:c(Na+)>c(SO42-)=c(NH4+)>c(OH-)=c(H+) | |
| D. | 等浓度、等体积的Na2CO3和NaHCO3混合:$\frac{c(HC{{O}_{3}}^{-})}{c({H}_{2}C{O}_{3})}$>$\frac{c(C{{O}_{3}}^{2-})}{c(HC{{O}_{3}}^{-})}$ |
18.Fe2O3在工业上有重要的用途,可发生如图所示的一系列反应.下列说法正确的是( )
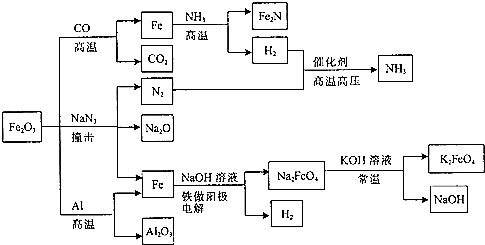

| A. | Fe2O3与Al的反应属于吸热反应 | |
| B. | Fe2O3与NaN3反应,每消耗1molFe2O3产生9molN2 | |
| C. | Fe2O3与CO的反应属于置换反应 | |
| D. | 常温下K2FeO4在水中的溶解度比Na2FeO4的大 |
2.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1mol铁与足量的盐酸完全反应,铁失去的电子数为0.3NA | |
| B. | 3.4g NH3中含原子总数目为0.6NA | |
| C. | 新制的含NA个Fe(OH)3分子的氢氧化铁胶体中,含有胶粒的物质的量为1mol | |
| D. | 23gNO2和N2O4的混合气体中含有原子总数1.5NA |
19.反应①Fe(s)+CO2(g)?FeO(s)+CO(g)△H1=akJ•mol-1,平衡常数为K;反应②CO(g)+$\frac{1}{2}$O2(g)?CO2(g)△H2=bkJ•mol-1.测得在不同温度下,K值如表:
(1)若500℃时进行反应①,CO2起始浓度为2mol/L,CO的平衡浓度为1mol/L.
(2)反应①中的a大于 0(填“大于”、“小于”或“等于”).
(3)700℃时反应①达到平衡,要使得该平衡向右移动,其他条件不变时,可以采取的措施有(填序号).
A.缩小反应器体积 B.通入CO2 C.升高温度到 900℃D.使用合适的催化剂
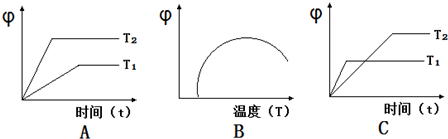
(4)如图图象符合反应①的是(填序号)(图中φ是混合物中CO的含量;T为温度).
(5)反应③2Fe(s)+O2(g)═2FeO(s)△H3=2(a+b)kJ•mol-1.
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
(2)反应①中的a大于 0(填“大于”、“小于”或“等于”).
(3)700℃时反应①达到平衡,要使得该平衡向右移动,其他条件不变时,可以采取的措施有(填序号).
A.缩小反应器体积 B.通入CO2 C.升高温度到 900℃D.使用合适的催化剂
(4)如图图象符合反应①的是(填序号)(图中φ是混合物中CO的含量;T为温度).

(5)反应③2Fe(s)+O2(g)═2FeO(s)△H3=2(a+b)kJ•mol-1.
16.已知三氧化硫的熔点为16.8℃,沸点为44℃,下列有关三氧化硫的说法中,正确的是( )
| A. | 常温下SO3是液体 | |
| B. | 标准状况下,1 mol SO3的体积约为22.4L | |
| C. | SO3与CaO反应生成CaSO3 | |
| D. | SO2遇空气即生成SO3 |
9.列实验与对应示意图的关系正确的是( )
| A | B | C | D |
| NaAlO2溶液中逐滴滴加盐酸至过量 | AlCl3溶液中逐滴滴加氨水至过量 | 明矾[KAl(SO4)2•12H2O]溶液中逐滴滴加Ba(OH)2溶液至过量 | 澄清石灰水中缓慢通入CO2至过量 |
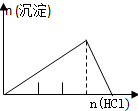 | 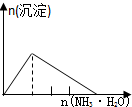 | 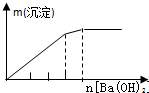 | 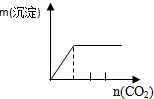 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
 ;
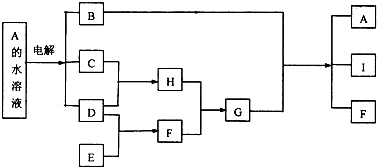
; 某课外活动小组同学用如图装置进行实验,一段时间后在C电极表面有铜析出,试回答下列问题.
某课外活动小组同学用如图装置进行实验,一段时间后在C电极表面有铜析出,试回答下列问题.