题目内容
Ⅰ.硫酸的消费量常被作为有关国家工业发达水平的一种标志,下表为接触法制硫酸时,温度和压强对SO2转化率的影响:
(1)硫酸工业在国民经济中占有重要的地位,请写出它的两种重要用途: 、 .
(2)工业中催化氧化SO2采用常压而不用高压,理由是 .
Ⅱ.实验室中,用如图1所示装置及所给药品(图中部分夹持仪器已略去)探究工业制硫酸接触室中的反应,并收集得到SO3.已知SO3熔点为16.8℃,沸点44.8℃,且SO3遇水剧烈反应.
(1)写出A装置中制取氧气的化学方程式 .
(2)B装置的作用除了将气体充分混合外,还有:① ,② .
(3)加热硬质玻璃管时,若不断升高温度,对SO2和O2生成SO3的化学反应有何影响: .
(4)本实验装置虚框处还需接一装置,甲、乙、丙三同学分别设计了如图2a、b、c三套装置,你认为不合理的是 ,理由是 .
| 压强/Mpa 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
(2)工业中催化氧化SO2采用常压而不用高压,理由是
Ⅱ.实验室中,用如图1所示装置及所给药品(图中部分夹持仪器已略去)探究工业制硫酸接触室中的反应,并收集得到SO3.已知SO3熔点为16.8℃,沸点44.8℃,且SO3遇水剧烈反应.

(1)写出A装置中制取氧气的化学方程式
(2)B装置的作用除了将气体充分混合外,还有:①
(3)加热硬质玻璃管时,若不断升高温度,对SO2和O2生成SO3的化学反应有何影响:
(4)本实验装置虚框处还需接一装置,甲、乙、丙三同学分别设计了如图2a、b、c三套装置,你认为不合理的是
考点:工业制取硫酸,性质实验方案的设计
专题:实验设计题,元素及其化合物
分析:Ⅰ(1)根据硫酸的性质分析;
(2)根据表中数据分析;
Ⅱ(1)双氧水在二氧化锰催化作用下能较快的生成氧气;
(2)把O2和SO2通入浓硫酸,能干燥气体,还可以控制速率;
(3)根据温度对速率和平衡的影响分析;
(4)根据三氧化硫的性质分析.
(2)根据表中数据分析;
Ⅱ(1)双氧水在二氧化锰催化作用下能较快的生成氧气;
(2)把O2和SO2通入浓硫酸,能干燥气体,还可以控制速率;
(3)根据温度对速率和平衡的影响分析;
(4)根据三氧化硫的性质分析.
解答:
解:Ⅰ(1)浓硫酸具有吸水性,可以作干燥剂,具有强氧化性可以作氧化剂,具有酸性有多种用途,
故答案为:化学试剂、干燥剂;
(2)由表中数据可知,常压时SO2的转化率已经很高,若加压对设备要求高,增大投资和能量消耗,
故答案为:常压时SO2的转化率已经很高,若加压对设备要求高,增大投资和能量消耗;
Ⅱ(1)双氧水在二氧化锰催化作用下能较快的生成氧气,所以A中的方程式为:2H2O2
2H2O+O2↑;故答案为:2H2O2
2H2O+O2↑;
(2)把O2和SO2通入浓硫酸,能干燥气体,还可以通过观察气泡来控制通入的气体的速率;
故答案为:干燥气体,观察气泡以便控制O2和SO2的流速;
(3)加热硬质玻璃管时,若不断升高温度,则反应速率加快,由于二氧化硫与氧气的反应是放热反应,升高温度,平衡逆移,二氧化硫的转化率会降低;
故答案为:①加快反应速率②SO2的转化率降低;
(4)三氧化硫与水反应生成硫酸,b装置中为氢氧化钠溶液,溶液中的水蒸气能进入U形管与三氧化硫接触而反应,所以不能选用b装置;
故答案为:b;b中挥发的水蒸气与D中SO3晶体剧烈反应.
故答案为:化学试剂、干燥剂;
(2)由表中数据可知,常压时SO2的转化率已经很高,若加压对设备要求高,增大投资和能量消耗,
故答案为:常压时SO2的转化率已经很高,若加压对设备要求高,增大投资和能量消耗;
Ⅱ(1)双氧水在二氧化锰催化作用下能较快的生成氧气,所以A中的方程式为:2H2O2
| ||
| ||
(2)把O2和SO2通入浓硫酸,能干燥气体,还可以通过观察气泡来控制通入的气体的速率;
故答案为:干燥气体,观察气泡以便控制O2和SO2的流速;
(3)加热硬质玻璃管时,若不断升高温度,则反应速率加快,由于二氧化硫与氧气的反应是放热反应,升高温度,平衡逆移,二氧化硫的转化率会降低;
故答案为:①加快反应速率②SO2的转化率降低;
(4)三氧化硫与水反应生成硫酸,b装置中为氢氧化钠溶液,溶液中的水蒸气能进入U形管与三氧化硫接触而反应,所以不能选用b装置;
故答案为:b;b中挥发的水蒸气与D中SO3晶体剧烈反应.
点评:本题考查了硫酸的性质,氧气的制备原理,温度对速率和平衡的影响等,考查的知识点较多,难度一般.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
下列过程所包含的有机化学反应中,不属于氧化反应的是( )
| A、烯烃使酸性高锰酸钾溶液褪色 |
| B、在家中燃烧液化石油气做饭 |
| C、乙酸与乙醇反应生成乙酸乙酯 |
| D、用装有酸性重铬酸钾的装置检验司机是否酒后驾车 |
下列各组中的离子,能在溶液中大量共存的是( )
| A、Ba2+、OH-、NO3-、Na+ |
| B、NH4+、OH-、SO42-、K+ |
| C、Ca2+、H+、Cl-、CO32- |
| D、Cu2+、SO42-、Ba2+、Cl- |
 设nA为阿伏加德罗常数的值,下列叙述正确的是( )
设nA为阿伏加德罗常数的值,下列叙述正确的是( )| A、常温常压下,16g14CH4所含中子数目为8nA |
| B、标准状况下,22.4 LCCl4所含分子数目为nA |
| C、1 L 0.5 mol?L-1的CH3COONa溶液中所含的CH3COO-离子数目为0.5nA |
| D、6.2g白磷(分子式为P4,分子结构如图所示)所含P-键数目为0.3nA |

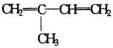 与 CH2=CH2 发生加成反应产物的结构简式(或键线式)
与 CH2=CH2 发生加成反应产物的结构简式(或键线式)
 小明同学在学习“硫酸及其盐的某些性质与用途”的过程中,进行如下实验探究.
小明同学在学习“硫酸及其盐的某些性质与用途”的过程中,进行如下实验探究.