题目内容
下列离子方程式中正确的是( )
|
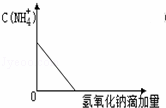
| A. | NH4HCO3溶液与过量NaOH溶液反应:NH4++OH﹣→NH3↑+2H2O |
|
| B. | 向FeBr2溶液中通入Cl2,当n(FeBr2)=n(Cl2)时:2Fe2++4Br﹣+3Cl2→2Fe3++2Br2+6Cl﹣ |
|
| C. | 向FeI2溶液中通入Cl2,当n(FeI2):n(Cl2)=1:1时:2I﹣+Cl2→I2+2Cl﹣ |
|
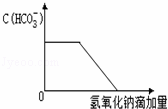
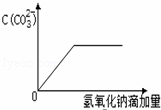
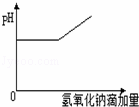
| D. | 向烧碱溶液中通入CO2,当n(NaOH):n(CO2)=3:2时:OH﹣+CO2→HCO3﹣ |
| 离子方程式的书写.. | |
| 专题: | 离子反应专题. |
| 分析: | A.漏写碳酸氢根离子与碱的反应; B.当n(FeBr2)=n(Cl2)时,亚铁离子全部被氧化,溴离子一半被氧化; C.当n(FeI2):n(Cl2)=1:1时,碘离子全部被氧化; D.n(NaOH):n(CO2)=3:2时,生成等量的碳酸钠、碳酸氢钠. |
| 解答: | 解:A.A.漏写碳酸氢根离子与碱的反应,离子反应为HCO3﹣+NH4++2OH﹣=NH3.H2O+CO32﹣+H2O,故A错误; B.当n(FeBr2)=n(Cl2)时,亚铁离子全部被氧化,溴离子一半被氧化,则离子反应为2Fe2++2Br﹣+2Cl2=2Fe3++Br2+4Cl﹣,故B错误; C.当n(FeI2):n(Cl2)=1:1时,碘离子全部被氧化,离子反应为2I﹣+Cl2=I2+2Cl﹣,故C正确; D.n(NaOH):n(CO2)=3:2时,生成等量的碳酸钠、碳酸氢钠,离子反应为3OH﹣+2CO2=HCO3﹣+CO32﹣+H2O,故D错误; 故选C. |
| 点评: | 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及与量有关的离子反应考查,注意优先氧化为解答的难点,题目难度中等. |

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案