题目内容
在2FeCl3+2KI═2FeCl2+2KCl+I2反应中:
(1)______元素被氧化,______是还原产物
(2)该反应的离子方程式为:______
(3)FeCl3的氧化性______I2的氧化性(填“>”、“<”).
(4)请用“双线桥法”标出该反应电子转移的方向和数目.
解:(1)在2FeCl3+2KI═2FeCl2+2KCl+I2反应中,碘元素化合价从-1价变化为0价,化合价升高时做还原剂,KI被氧化发生氧化反应,铁元素化合价从+3价降低到+2价,化合价降低做氧化剂,被还原得到还原产物FeCl2,故答案为:I;FeCl2;
(2)该反应的离子方程式为:2Fe3++2I-=2Fe2++I2,故答案为:2Fe3++2I-=2Fe2++I2;
(3)氧化还原反应中的氧化剂FeCl3的氧化性大于氧化产物I2,故答案为:>;
(4)铁元素化合价从+3价变化为+2价得到电子;碘元素化合价从-1价变化为0价,用双线桥标注电子转移: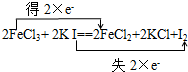 ,
,
故答案为: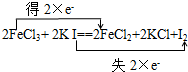 .
.
分析:(1)依据反应前后元素化合价变化分析,元素化合价升高的失电子做还原剂发生氧化反应,元素化合价降低的得到电子发生还原反应做氧化剂,得到还原产物;
(2)依据离子方程式的书写方法写出离子方程式,遵循电荷守恒,原子守恒;
(3)氧化还原反应中的氧化剂的氧化性大于氧化产物;
(4)依据元素化合价变化计算元素原子得失电子数,标明得失电子的方向和数目.
点评:本题考查了氧化还原反应的概念分析判断,元素化合价的变化分析是解题关键,强弱规律的掌握和电子转移的标注需要熟练掌握基础知识.
(2)该反应的离子方程式为:2Fe3++2I-=2Fe2++I2,故答案为:2Fe3++2I-=2Fe2++I2;
(3)氧化还原反应中的氧化剂FeCl3的氧化性大于氧化产物I2,故答案为:>;
(4)铁元素化合价从+3价变化为+2价得到电子;碘元素化合价从-1价变化为0价,用双线桥标注电子转移:
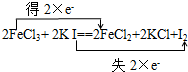 ,
,故答案为:
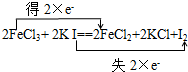 .
.分析:(1)依据反应前后元素化合价变化分析,元素化合价升高的失电子做还原剂发生氧化反应,元素化合价降低的得到电子发生还原反应做氧化剂,得到还原产物;
(2)依据离子方程式的书写方法写出离子方程式,遵循电荷守恒,原子守恒;
(3)氧化还原反应中的氧化剂的氧化性大于氧化产物;
(4)依据元素化合价变化计算元素原子得失电子数,标明得失电子的方向和数目.
点评:本题考查了氧化还原反应的概念分析判断,元素化合价的变化分析是解题关键,强弱规律的掌握和电子转移的标注需要熟练掌握基础知识.

练习册系列答案
相关题目
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O  4NO+6H2O
4NO+6H2O Na2SO4+2NH3↑+2H2O
Na2SO4+2NH3↑+2H2O Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl