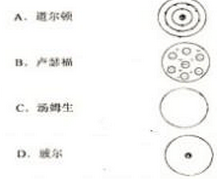
题目内容
19.有7.8gA和0.1molB恰好完全反应后,生成10.6gC和1.6gD,则B的摩尔质量是( )| A. | 44g/mol | B. | 78g/mol | C. | 106g/mol | D. | 88g/mol |
分析 根据质量守恒定律计算生成的E物质的质量,再利用M=$\frac{m}{n}$计算E的摩尔质量.
解答 解:7.8gA和0.1molB恰好完全反应后,生成10.6gC和1.6gD,由质量守恒定律可知,B的质量为1.6g+10.6g-7.8g=4.4g,
B的物质的量为0.1mol,则B的摩尔质量为$\frac{4.4g}{0.1mol}$=44g/mol,
故选A.
点评 本题考查化学方程式计算、摩尔质量的计算,关键数据根据质量守恒定律计算E的质量,熟练掌握物质的量有关计算,注意摩尔质量的单位,比较基础.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.下列装置能实现实验目的是( )
| A. | 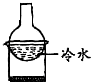 加热烧杯,除去NH4Cl中混有的I2 | B. | 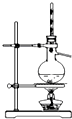 分离溴苯与苯的混合物 | ||
| C. | 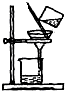 分离淀粉与葡萄糖的混合液 | D. | 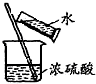 稀释浓硫酸 |
14.下列说法正确的是( )
| A. | 1mL pH=2 的醋酸溶液加水稀释到10mL,pH 变为3 | |
| B. | 常温下,Na2CO3溶液中加水稀释时,$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$增大 | |
| C. | 向氯水中加入少量NaOH 溶液,一定有c(Na+)=c(Cl-)+c(ClO-) | |
| D. | NH4Cl 溶液稀释过程中,c(NH4+)与c(NH3•H2O)之和始终保持不变 |
4.下列说法正确的是( )
| A. | 金属钠取用时要用镊子.多余的钠不能放回瓶中 | |
| B. | 用pH试纸检验气体时应预先润湿 | |
| C. | 用苯苹取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| D. | 可用新制的银氨溶液鉴别两瓶失去标签的乙醛和葡萄糖溶液 |
11.已知向KI溶液中通入过量Cl2时,生成的I2可进一步氧化成IO3-,若通入Cl2的物质的量为amol,溶液中KI的物质的量为bmol(不考虑单质与水的反应),下列说法不正确的是( )
| A. | I2与Cl2反应的离子方程式为:I2+5Cl2+6H2O=2IO3-+12H++10Cl- | |
| B. | 当a=3b时,发生反应的离子方程式为:I-+3Cl2+3H2O=IO3-+6Cl-+6H+ | |
| C. | 当a=2b时,发生反应的离子方程式为:5I-+10Cl2+9H2O=3IO3-+20Cl-+I2+18H+ | |
| D. | 若反应后溶液中I2与IO3-的物质的量之比为1:1,则反应中转移电子3.5bmol |
17.下列做法不符合绿色化学原则的是( )
| A. | 提高能源的利用率 | B. | 应用无毒无害的催化剂 | ||
| C. | 使用可以再生的资源 | D. | 工业及生活废水的任意排放 |
18.氧族元素的氢化物的沸点如表:
下列关于氧族元素氢化物的沸点高低的分析和推断中,正确的是( )
| H2O | H2S | H2Se | H2Te |
| 100℃ | -60.75℃ | -41.5℃ | -1.8℃ |
| A. | 氧族元素氢化物沸点高低与范德华力的大小无关 | |
| B. | 范德华力一定随相对分子质量的增大而减小 | |
| C. | 水分子间可能还存在一种特殊的分子间作用力 | |
| D. | 水分子间存在共价键,加热时较难断裂 |