题目内容
5.按要求写出相关的方程式:(1)写出电解饱和食盐水的化学方程式2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑
(2)氯化铵溶液呈现酸碱性的离子方程式NH4++H2O?NH3•H2O+H+
(3)乙醇和氧气以KOH为电解质的溶液形成的燃料电池的负极电极反应式C2H5OH+16OH--12e-=2CO32-+11H2O.
分析 (1)电解饱和食盐水生成氯气、氢气和氢氧化钠;
(2)氯化铵溶液中氨根离子水解生成一水合氨和氯化氢;
(3)乙醇在负极发生氧化反应生成碳酸根离子和水.
解答 解:(1)电解饱和食盐水阳极上氯离子失电子发生氧化反应得到氯气,电解反应2Cl--2e-=Cl2↑,阴极上氢离子得到电子生成氢气,电解反应为2H++2e-=H2↑,总反应为2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑,
故答案为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑;
(2)氯化铵溶液呈现酸碱性的离子方程式:NH4++H2O?NH3•H2O+H+,故答案为:NH4++H2O?NH3•H2O+H+;
(3)乙醇在负极发生氧化反应生成碳酸根离子和水,离子方程式为:C2H5OH+16OH--12e-=2CO32-+11H2O,故答案为:C2H5OH+16OH--12e-=2CO32-+11H2O.
点评 本题考查了离子方程式、化学方程式的书写,明确反应的实质是解题关键,注意原子个数守恒、电荷数守恒.

练习册系列答案
相关题目
9.设NA为阿伏加德罗常数的值.下列说法中正确的是( )
| A. | 过氧化钠用作呼吸面具中的供氧剂,每生成0.1molO2,转移电子的数目为0.4NA | |
| B. | 将1mL1mol/LFeCl3溶液逐滴加入沸水,制得红褐色Fe(OH)3胶体,所含胶粒的数目是1×10-3NA | |
| C. | 标准状况下,0.1molCl2溶于水,转移电子的数目为0.1NA | |
| D. | 7.8gNa2S和Na2O2的混合物中,含有的阴离子数目为0.1NA |
16. 硫酸是工业生产中重要的产品之一,在很多领域都有重要用途.回答下列问题:
硫酸是工业生产中重要的产品之一,在很多领域都有重要用途.回答下列问题:
(1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,反应的化学方程式为4FeS2+11O2 $\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2;该反应在沸腾炉(填设备名称)中进行.
(2)为了有利于SO2转化为SO3,且能充分利用热能,可采用在有多层催化剂且有热交换器的接触室(填设备名称)中进行反应.在如图所示的装置中,C处流出的气体有SO3、SO2、O2,SO3进入吸收塔(填设备名称)中用98.3%的H2SO4吸收,得到浓硫酸或发烟硫酸.
(3)实验测得:SO2生成SO3的转化率与温度、压强的关系如表所示.已知400~600℃催化剂的催化效果较好,结合生产实际,选择最合适的生产条件是400℃,1个标准大气压
(4)欲提高SO2的反应速率和转化率,下列措施可行的是B(填选项字母).
A.向装置中通入氮气且保持体积不变
B.向装置中通入稍过量氧气且保持体积不变
C.添加更多的催化剂
D.降低温度,及时转移SO3
(5)吸收塔排出的尾气中,若SO2的含量超过500μL•L-1,就要加以处理,处理方法之一是用氨水洗涤烟气脱硫,用足量氨水吸收尾气中SO2的化学方程式为2NH3•H2O+SO2=(NH4)2SO3+H2O.
 硫酸是工业生产中重要的产品之一,在很多领域都有重要用途.回答下列问题:
硫酸是工业生产中重要的产品之一,在很多领域都有重要用途.回答下列问题:(1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,反应的化学方程式为4FeS2+11O2 $\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2;该反应在沸腾炉(填设备名称)中进行.
(2)为了有利于SO2转化为SO3,且能充分利用热能,可采用在有多层催化剂且有热交换器的接触室(填设备名称)中进行反应.在如图所示的装置中,C处流出的气体有SO3、SO2、O2,SO3进入吸收塔(填设备名称)中用98.3%的H2SO4吸收,得到浓硫酸或发烟硫酸.
(3)实验测得:SO2生成SO3的转化率与温度、压强的关系如表所示.已知400~600℃催化剂的催化效果较好,结合生产实际,选择最合适的生产条件是400℃,1个标准大气压
| 压强 SO2转化率 温度 | 1.0×105Pa | 5.0×105Pa | 1.0×106Pa | 1.5×106Pa |
| 400℃ | 0.9961 | 0.9972 | 0.9984 | 0.9989 |
| 500℃ | 0.9675 | 0.9767 | 0.9852 | 0.9894 |
| 600℃ | 0.8528 | 0.8897 | 0.9276 | 0.9468 |
A.向装置中通入氮气且保持体积不变
B.向装置中通入稍过量氧气且保持体积不变
C.添加更多的催化剂
D.降低温度,及时转移SO3
(5)吸收塔排出的尾气中,若SO2的含量超过500μL•L-1,就要加以处理,处理方法之一是用氨水洗涤烟气脱硫,用足量氨水吸收尾气中SO2的化学方程式为2NH3•H2O+SO2=(NH4)2SO3+H2O.
13.蒸馏水的制取及检验
| 实验目的 | 实验操作 | 现象 | 结论 |
| 自来水中离子检验 | 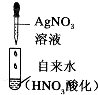 | 出现不溶于稀HNO3的沉淀 | 自来水中含氯离子 |
| 水的提纯 | 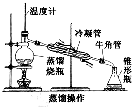 | 蒸馏烧瓶中水沸腾,冷凝管中有无色液体凝结,并通过冷凝管流入锥形瓶中 | 锥形瓶中收集到无色液体 |
| 蒸馏水中杂质离子的检验 | 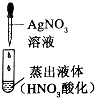 | 无明显现象 | 蒸馏水中不含氯离子 |
20.化学与科学、技术、社会、环境密切相关.下列有关说法中正确的是( )
| A. | 朝鲜第三次核试验产生的放射性物质的衰变为化学变化 | |
| B. | 燃烧化石燃料排放的废气中含大量CO2、SO2,形成酸雨 | |
| C. | 为防止垃圾污染城市,可采用露天焚烧或深埋的方法进行处理 | |
| D. | 用高纯度二氧化硅制作的光导纤维遇强碱会“断路” |
10.为使人们确知含碘物质的存在,研究性学习小组同学设计了一种简便的检验方法,利用该物质在酸性条件下与KI反应有单质碘生成的性质,选用下列生活常见的物质就可完成.请你从下列物质中选出合适的一组( )
①自来水 ②食醋 ③淀粉 ④食糖 ⑤碘化钾试纸 ⑥碘酒.
①自来水 ②食醋 ③淀粉 ④食糖 ⑤碘化钾试纸 ⑥碘酒.
| A. | ①③④⑤ | B. | ②③④⑤ | C. | ①③⑤⑥ | D. | ①②③⑤ |
17.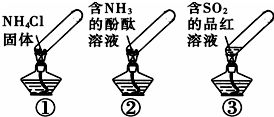 “封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )
 “封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )| A. | 加热时,①上部汇集了固体NH4Cl,说明NH4Cl的热稳定性比较好 | |
| B. | 加热时,②溶液褪色或红色变浅,冷却后又都变为红色 | |
| C. | 加热时,③溶液褪色或红色变浅,冷却后又都变为红色 | |
| D. | 三个“封管实验”中所发生的化学反应都是可逆反应 |
14.低温脱氮技术可用于处理废气中的氮氧化物.发生的化学反应为:4NH3(g)+6NO(g)$?_{△}^{催化剂}$5N2(g)+6H2O(g)+Q,在恒容密闭容器中,下列有关说法正确的是( )
| A. | 该反应是放热反应,降低温度将缩短反应达到平衡的时间 | |
| B. | 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 | |
| C. | 单位时间内消耗NO和N2的物质的量比为6:5时,反应达到平衡 | |
| D. | 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
15.下列各对物质中,互为同分异构体的是( )
| A. | CH3-CH2-CH3和CH3-CH2-CH2-CH3 | B. |  | ||
| C. | 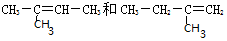 | D. | 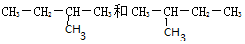 |