题目内容
6.(1)下列化学用语均有错误,请将正确的化学用语填在相应的横线上氯元素Cl,2个氮分子2N2,铁离子Fe2+Fe3+(2)填表:(类别选填“单质”、“氧化物”、“酸”、“碱”、“盐:
| 名称 | 氢氧化镁 | 银 | |
| 化学式 | HNO3 | Mg(OH)2 | |
| 类别 | 酸 | 单质 |
分析 (1)据元素符号通常用元素的拉丁名称的第一个字母(大写)来表示,如碳-C.如果几种元素名称的第一个字母相同,就在第一个字母(必须大写)后面加上元素名称中另一个字母(必须小写)以示区别;进行解答;
根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,进行解答;
根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;进行解答.
(2)HNO3俗称硝酸;电离出的阴离子全部是氢氧根的化合物为碱;单质银的化学式为Ag.
解答 解:(1)根据元素符号通常用元素的拉丁名称的第一个字母(大写)来表示,如碳-C.如果几种元素名称的第一个字母相同,就在第一个字母(必须大写)后面加上元素名称中另一个字母(必须小写)以示区别;可知氯元素应表示为:Cl;根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,因此2个氮分子表示为:2N2;
根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;因此铁离子表示为:Fe3+;
(2)HNO3俗称硝酸,是一种强酸;电离出的阴离子全部是氢氧根的化合物为碱,故氢氧化镁属于碱;单质银的化学式为Ag.故答案为:
| 名称 | 硝酸 | ||
| 化学式 | Ag | ||
| 类别 | 碱 |
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
12.为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施.化学反应的焓变通常用实验进行测定,也可进行理论推算.
(1)实验测得,4.6g乙醇(CH3CH2OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出136.68kJ的热量,试写出表示乙醇燃烧热的热化学方程式:CH3CH2OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H=-1366.8kJ/mol
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键形成的过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键双会释放能量.
已知反应N2(g)+3H2(g)═2NH3(g)△H=akJ•mol-1.
试根据表中所列键能数据计算a的数值:-93
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(石墨,s)+O2(g)═CO2(g)H1=-393.5kJ•mol-1①2H2(g)+O2(g)═2H2O(l)H2=-571.6kJ•mol-1②2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1③
根据盖期定律,计算298K时由C(石墨,s)和H2(g)生成1molC2H2(g)反应的焓变+227.7kJ•mol-.(写出简要的计算过程).
(1)实验测得,4.6g乙醇(CH3CH2OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出136.68kJ的热量,试写出表示乙醇燃烧热的热化学方程式:CH3CH2OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H=-1366.8kJ/mol
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键形成的过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键双会释放能量.
已知反应N2(g)+3H2(g)═2NH3(g)△H=akJ•mol-1.
| 化学键 | H-H | N-H | N≡N |
| 键能(kJ•mol-1) | 436 | 391 | 945 |
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(石墨,s)+O2(g)═CO2(g)H1=-393.5kJ•mol-1①2H2(g)+O2(g)═2H2O(l)H2=-571.6kJ•mol-1②2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1③
根据盖期定律,计算298K时由C(石墨,s)和H2(g)生成1molC2H2(g)反应的焓变+227.7kJ•mol-.(写出简要的计算过程).
13.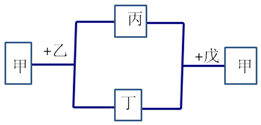 短周期元素W、X、Y、Z的原子序数依次增加.甲为元素Z的单质,通常为淡黄色固体,乙、丙、丁、戊为这些元素组成的化合物,常温下0.1mol•L-1乙溶液pH为13,戊为Z的最高价氧化物的水化物.上述物质间的转化关系如图所示(部分产物及反应条件已略去).下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.甲为元素Z的单质,通常为淡黄色固体,乙、丙、丁、戊为这些元素组成的化合物,常温下0.1mol•L-1乙溶液pH为13,戊为Z的最高价氧化物的水化物.上述物质间的转化关系如图所示(部分产物及反应条件已略去).下列说法正确的是( )
 短周期元素W、X、Y、Z的原子序数依次增加.甲为元素Z的单质,通常为淡黄色固体,乙、丙、丁、戊为这些元素组成的化合物,常温下0.1mol•L-1乙溶液pH为13,戊为Z的最高价氧化物的水化物.上述物质间的转化关系如图所示(部分产物及反应条件已略去).下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.甲为元素Z的单质,通常为淡黄色固体,乙、丙、丁、戊为这些元素组成的化合物,常温下0.1mol•L-1乙溶液pH为13,戊为Z的最高价氧化物的水化物.上述物质间的转化关系如图所示(部分产物及反应条件已略去).下列说法正确的是( )| A. | 简单离子的半径大小X<Y<Z | |
| B. | 化合物乙中含离子键和非极性共价键 | |
| C. | W与Z形成的化合物常温常压下呈液态 | |
| D. | 图中生成甲的离子方程式为6H++SO32-+2S2-=3S↓+3H2O |
14.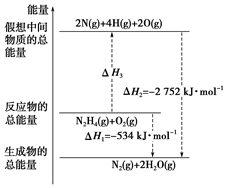 肼(H2N-NH2)是一种高能燃料,有关化学反应的能量变化如图所示.已知断裂1mol 化学键所需的能量(kJ):N≡N 为942、O=O为500、N-N为154,则断裂1mol N-H 键所需的能量(kJ)是( )
肼(H2N-NH2)是一种高能燃料,有关化学反应的能量变化如图所示.已知断裂1mol 化学键所需的能量(kJ):N≡N 为942、O=O为500、N-N为154,则断裂1mol N-H 键所需的能量(kJ)是( )
 肼(H2N-NH2)是一种高能燃料,有关化学反应的能量变化如图所示.已知断裂1mol 化学键所需的能量(kJ):N≡N 为942、O=O为500、N-N为154,则断裂1mol N-H 键所需的能量(kJ)是( )
肼(H2N-NH2)是一种高能燃料,有关化学反应的能量变化如图所示.已知断裂1mol 化学键所需的能量(kJ):N≡N 为942、O=O为500、N-N为154,则断裂1mol N-H 键所需的能量(kJ)是( )| A. | 194 | B. | 391 | C. | 516 | D. | 685 |
1.已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中的信息,回答下列问题:
(1)表中硫酸的质量分数为$\frac{98{c}_{1}}{1000{ρ}_{1}}$(不写单位,用含c1、ρ1的代数式表示).
(2)物质的量浓度为c1mol•L-1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为0.5c1mol•L-1.
(3)物质的量浓度为c2mol•L-1的氨水与$\frac{1}{5}$c2mol•L-1的氨水等质量混合,所得溶液的密度大于(填“大于”、“小于”或“等于”,下同) ρ2g•cm-3,所得溶液的物质的量浓度大于$\frac{3}{5}$c2mol•L-1(设混合后溶液的体积变化忽略不计)
(4)若将稀硫酸与氨水混合,写出其反应的离子方程式NH3•H2O+H+=NH4++H2O.
| 溶质的物质的量浓度/mol•L-1 | 溶液的密度/g•cm-3 | 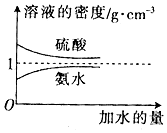 | |
| 硫酸 | c1 | ρ1 | |
| 氨水 | c2 | ρ2 |
(2)物质的量浓度为c1mol•L-1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为0.5c1mol•L-1.
(3)物质的量浓度为c2mol•L-1的氨水与$\frac{1}{5}$c2mol•L-1的氨水等质量混合,所得溶液的密度大于(填“大于”、“小于”或“等于”,下同) ρ2g•cm-3,所得溶液的物质的量浓度大于$\frac{3}{5}$c2mol•L-1(设混合后溶液的体积变化忽略不计)
(4)若将稀硫酸与氨水混合,写出其反应的离子方程式NH3•H2O+H+=NH4++H2O.
11.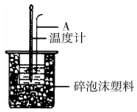 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下:
①量取50mL 0.25mol/L H2SO4溶液倒入小烧杯中,测量温度;
②量取50mL 0.55mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度.
请回答:
(1)如图所示,仪器A的名称是环形玻璃搅拌棒;
(2)设溶液的密度均为1g•cm-3,中和后溶液的比热容c=4.18J•(g•℃)-1,请根据实验数据写出该中和热的热化学方程式$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-56.0kJ/mol
(3)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是abc(填字母)
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(4)已知:CH3COOH(aq)与NaOH(aq)反应的△H=-12.1kJ•mol-1;HCl(aq)与NaOH(aq)反应的△H=-55.6kJ•mol-1.则CH3COOH在水溶液中电离的△H等于C
A.-67.7kJ•mol-1 B.-43.5kJ•mol-1C.+43.5kJ•mol-1 D.+67.7kJ•mol-1.
 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下:①量取50mL 0.25mol/L H2SO4溶液倒入小烧杯中,测量温度;
②量取50mL 0.55mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度.
请回答:
(1)如图所示,仪器A的名称是环形玻璃搅拌棒;
(2)设溶液的密度均为1g•cm-3,中和后溶液的比热容c=4.18J•(g•℃)-1,请根据实验数据写出该中和热的热化学方程式$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-56.0kJ/mol
 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 25.0 | 25.2 | 28.5 | ||
| 2 | 24.9 | 25.1 | 28.3 | ||
| 3 | 25.5 | 26.5 | 31.8 | ||
| 4 | 25.6 | 25.4 | 29.0 | ||
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(4)已知:CH3COOH(aq)与NaOH(aq)反应的△H=-12.1kJ•mol-1;HCl(aq)与NaOH(aq)反应的△H=-55.6kJ•mol-1.则CH3COOH在水溶液中电离的△H等于C
A.-67.7kJ•mol-1 B.-43.5kJ•mol-1C.+43.5kJ•mol-1 D.+67.7kJ•mol-1.
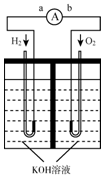 氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答: