题目内容
14.用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是( )| A. | 干燥的 | B. | 瓶塞不漏水的 | ||
| C. | 用待配溶液洗涤过的 | D. | 以上三项都符合的 |
分析 用容量瓶配制一定物质的量浓度的溶液,在使用前要先检查是否漏水,容量瓶中无论干燥与否,对实验结果没有影响,但不能用欲配制的溶液润洗过的,会导致误差偏大.
解答 解:A.用容量瓶配制一定物质的量浓度的溶液,容量瓶中无论干燥与否,对实验结果没有影响,故A错误;
B.容量瓶有塞子,塞子不能漏水,故B正确;
C.不能用欲配制的溶液润洗过的,会导致误差偏大,故C错误;
故选B.
点评 本题考查容量瓶的使用,题目难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
4.下列各组离子,能大量共存于同一溶液中的是( )
| A. | CO32-、H+、Na+、NO3- | B. | H+、Ag+、Cl-、SO42- | ||
| C. | K+、Na+、OH-、SO42- | D. | Ba2+、Ca2+、SO42-、OH- |
5.下列反应中水既不作氧化剂,也不作还原剂的是( )
| A. | 2Na十2H2O═=2NaOH十H2↑ | B. | 2H2O═2H2↑十O2↑ | ||
| C. | 2F2十2H2O═4HF十O2 | D. | SO3十H2O═H2S04 |
2.在pH为0的溶液中,能大量存在的离子组是( )
| A. | AlO2-、NH4+、K+、Na+ | B. | SO42-、NH4+、Al3+、Cl- | ||
| C. | HS-、S2-、K+、NH4+ | D. | NH4+、Na+、CO32-、Fe3+ |
9.某温度下重水中存在电离平衡D2O?D++OD-,D2O的离子积常数=1.0×10-12,若pD=-lgc(D+),该温度下有关分析不正确的是( )
| A. | 0.1 mol NaOD溶于重水制成1L溶液,pD=11 | |
| B. | 将pD为4的DCl的重水溶液稀释10倍,所得溶液pD为5 | |
| C. | 向30 mL 0.5mol•L-1NaOD的重水溶液中加入20 mL 0.5 mol•L-1DCl的重水溶液,所得溶液pD=10 | |
| D. | pD=10的NaOD的重水溶液中,由重水电离出的c(OD-)为1×10-10mol•L-1 |
19.同温同压下,加热NaHCO3至完全分解,放出的CO2用Na2O2来吸收,则NaHCO3与Na2O2的最佳物质的量之比为( )
| A. | 1:1 | B. | 1:2 | C. | 2:1 | D. | 2:3 |
6.已知25℃时有关弱酸的电离平衡常数:
则下列有关说法正确的是( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
| A. | 等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) | |
| B. | 将a mol•L-1 HCN溶液与a mol•L-1 NaOH溶液等体积混合,混合液中:c(OH-)>c(H+),c(Na+)>c(CN-) | |
| C. | 冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小 | |
| D. | NaHCO3和Na2CO3混合液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
4.某无色溶液X,由 Na+、Ag+、Ba2+、Al3+、AlO2-、Fe3+、CO32-、SO42-中的若干种离子组成,取溶液进行如图连续实验( )
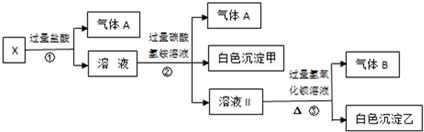

| A. | 气体A是CO2,白色沉淀甲是氢氧化铝 | |
| B. | 溶液中一定不含Ag+、Fe3+、SO42- | |
| C. | 溶液Ⅱ是硫酸钠、碳酸氢铵、氯化钠的混合物 | |
| D. | 溶液中一定存在的离子有Na+、CO32-、AlO2-和SO42- |