题目内容
4.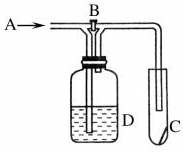 如图是一种试验某气体化学性质的实验装置,图中B为开关.若先打开B,在A处通入干燥的氯气,C中红色布条颜色无变化;当关闭B在A处通入干燥的氯气时,C中红色布条颜色褪去.则D瓶中盛有的溶液是( )
如图是一种试验某气体化学性质的实验装置,图中B为开关.若先打开B,在A处通入干燥的氯气,C中红色布条颜色无变化;当关闭B在A处通入干燥的氯气时,C中红色布条颜色褪去.则D瓶中盛有的溶液是( )| A. | 浓NaI溶液 | B. | 浓NaOH溶液 | C. | 饱和NaCl溶液 | D. | 浓硫酸 |
分析 先打开B,在A处通入干燥的氯气,C中红色布条颜色无变化;当关闭B在A处通入干燥的氯气时,C中红色布条颜色褪去,可知D中的试剂与氯气不反应,且氯气与水反应生成具有漂白性的HClO,以此来解答.
解答 解:NaI、NaOH均与氯气反应,浓硫酸干燥氯气,只有C中NaCl与氯气不反应,且氯气与水反应生成具有漂白性的HClO,符合题意,
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应和现象、装置的作用为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识的应用及实验评价性分析,题目难度不大.

练习册系列答案
相关题目
14.下列说法不正确的是( )
| A. | 次氯酸是一种弱酸是因为次氯酸不稳定,易分解 | |
| B. | 用氯气制漂白粉的主要目的是转变为较稳定,便于贮存的物质 | |
| C. | 漂白粉在空气中容易失效的原因是次氯酸钙易和空气中的水及二氧化碳反应 | |
| D. | 氯原子最外层有7个电子,故在化学反应中易结合一个电子而形成Cl- |
15.下列叙述正确的是( )
| A. | 标准状况下,两种气体的体积之比等于摩尔质量之比 | |
| B. | 常温常压下,两种气体的物质的量之比等于密度之比 | |
| C. | 同温同压下,两种气体的摩尔质量之比等于密度反比 | |
| D. | 同温同体积时,两种气体的物质的量之比等于压强之比 |
12.将锌片和铜片按图示方式插入稀硫酸中,下列结论正确的是( )
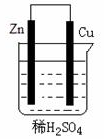

| A. | 将电能转换为化学能 | B. | 电子由铜片流出 | ||
| C. | 锌片时负极 | D. | 铜片逐渐被腐蚀 |
19.下列物质分类中,前者包括后者的是( )
| A. | 电解质 石墨 | B. | 胶体 分散系 | C. | 混合物 漂白粉 | D. | 碱性氧化物 CO2 |
9.实验过程中,不会产生气体的是( )
| A. | 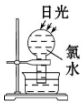 | B. | 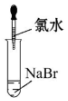 | C. | 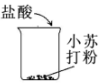 | D. | 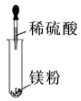 |
16.下列有关化学用语表示正确的是( )
| A. | 氯乙烯分子的结构简式:H3C-CH2Cl | B. | 硫原子的结构示意图: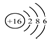 | ||
| C. | 过氧化钠的电子式: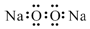 | D. | 中子数为10的氧原子:${\;}_{8}^{10}$O |
17.恒温、恒压下,1mol A和1mol B在一个容积可变的容器中发生如下反应:A(g)+2B(g)?2C(g),一段时间后达到平衡,生成a mol C,则下列说法中正确的是( )
| A. | 物质A、B的转化率之比为1:2 | |
| B. | 起始时刻和达平衡后容器中混合气体密度相等 | |
| C. | 当v正(A)=2v逆(C)时,可断定反应达到平衡状态 | |
| D. | 若起始时放入3 mol A和3 mol B,则达平衡时生成 3a mol C |