题目内容
运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义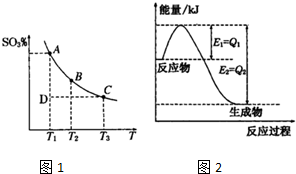
(1)硫酸生产中,SO2催化氧化生成SO3;2SO2(g)+O2(g)?2SO3(g),混合体系中SO3的百分含量和温度的关系如图1所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题,
①2SO2(g)+O2(g)?2SO3(g)的△H<0;若在恒温、恒压条件下向上述平衡体系中通人氦气,平衡 移动(填“向左”或“向右”)
②若温度为T1、T2,反应的平衡常数分别为K1,K2,则K1 K2;反应进行到状态D时,v正
v逆(填“>”“<”或“=”)
(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,
①如图2是一定的温度和压强下N2和H2反应生成lmolNH3过程中能量变化示意图,请写出工业合成氨的热化学方程式: (△H的数值用含字母Q1、Q2的代数式表示)
②氨气溶于水得到氨水,在25℃下,将a mol?L-1的氨水与b mol?L-1的盐酸等体积混合,反应后溶液显中性,则c(NH4+)=c(Cl-)请写出氨水的电离平衡常数表达式为 ,并用含a和b的代数式表示出该混合溶液中氨水的电离平衡常数为 .
(3)若在某浓度的氯化钡溶液VmL中,加入一定体积、物质的量浓度为0.0500mol/L的稀硫酸时,两者恰好完全反应,此时溶液的pH=3.试求:
①加入稀硫酸的体积 (用含V的计算式表示,设溶液混合时体积变化忽略不计);
②原氯化钡溶液的物质的量浓度.

(1)硫酸生产中,SO2催化氧化生成SO3;2SO2(g)+O2(g)?2SO3(g),混合体系中SO3的百分含量和温度的关系如图1所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题,
①2SO2(g)+O2(g)?2SO3(g)的△H<0;若在恒温、恒压条件下向上述平衡体系中通人氦气,平衡
②若温度为T1、T2,反应的平衡常数分别为K1,K2,则K1
v逆(填“>”“<”或“=”)
(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,
①如图2是一定的温度和压强下N2和H2反应生成lmolNH3过程中能量变化示意图,请写出工业合成氨的热化学方程式:
②氨气溶于水得到氨水,在25℃下,将a mol?L-1的氨水与b mol?L-1的盐酸等体积混合,反应后溶液显中性,则c(NH4+)=c(Cl-)请写出氨水的电离平衡常数表达式为
(3)若在某浓度的氯化钡溶液VmL中,加入一定体积、物质的量浓度为0.0500mol/L的稀硫酸时,两者恰好完全反应,此时溶液的pH=3.试求:
①加入稀硫酸的体积
②原氯化钡溶液的物质的量浓度.
考点:化学平衡的计算,热化学方程式,化学平衡的影响因素,弱电解质在水溶液中的电离平衡,酸碱混合时的定性判断及有关ph的计算
专题:基本概念与基本理论
分析:(1)①恒温、恒压条件下向上述平衡体系中通入氦气,体积应增大,反应混合物各组分的浓度降低,等效为降低压强,压强降低平衡向体积增大方向移动;
②由图可知,温度越高,混合体系中SO3的百分含量越小,说明升高温度平衡向逆反应进行,据此判断;D状态未达平衡,混合体系中SO3的百分含量小于平衡时的,反应向正反应进行建立平衡;
(2)①由图求出N2和H2反应生成1molNH3的反应热,再根据热化学反应方程式的书写要求解答;
②氨水的电离平衡常数为电离出离子的浓度积与溶质浓度的比值;
(3)①氯化钡与硫酸反应生成硫酸钡与HCl,反应中氢离子的物质的量不变,设加入稀硫酸的体积为xmL,利用氢离子物质的量列方程计算;
②氯化钡与硫酸反应生成硫酸钡与HCl,氯化钡的物质的量等于硫酸的物质的量,令氯化钡的浓度为ymol/L,列方程计算.
②由图可知,温度越高,混合体系中SO3的百分含量越小,说明升高温度平衡向逆反应进行,据此判断;D状态未达平衡,混合体系中SO3的百分含量小于平衡时的,反应向正反应进行建立平衡;
(2)①由图求出N2和H2反应生成1molNH3的反应热,再根据热化学反应方程式的书写要求解答;
②氨水的电离平衡常数为电离出离子的浓度积与溶质浓度的比值;
(3)①氯化钡与硫酸反应生成硫酸钡与HCl,反应中氢离子的物质的量不变,设加入稀硫酸的体积为xmL,利用氢离子物质的量列方程计算;
②氯化钡与硫酸反应生成硫酸钡与HCl,氯化钡的物质的量等于硫酸的物质的量,令氯化钡的浓度为ymol/L,列方程计算.
解答:
解:(1)①恒温、恒压条件下向上述平衡体系中通入氦气,体积应增大,反应混合物各组分的浓度降低,等效为降低压强,压强降低平衡向体积增大方向移动,即向左移动,故答案为:向左;
②由图可知,温度越高,混合体系中SO3的百分含量越小,说明升高温度平衡向逆反应进行,K值减小,故平衡常数K1>K2,D状态未达平衡,混合体系中SO3的百分含量小于平衡时的,反应向正反应进行建立平衡,所以V正>V逆,
故答案为:>;>;
(2)①由图可知,N2和H2反应生成1molNH3放出的热量为(Q2-Q1)kJ,该反应的热化学反应方程式为N2(g)+3H2(g)?2NH3(g)△H=-2(Q2-Q1)kJ?mol-1,
故答案为:N2(g)+3H2(g)?2NH3(g)△H=-2(Q2-Q1)kJ?mol-1.
②根据氨水的电离平衡常数为电离出离子的浓度积与溶质浓度的比值,则氨水中的电离常数为K=
,将a mol?L-1的氨水与b mol?L-1的盐酸等体积混合,反应后溶液显中性,则c(NH4+)=c(Cl-),则c(H+)=c(OH-)=10-7,
K=
=
,
故答案为:K=
;
;
(3)①氯化钡与硫酸反应生成硫酸钡与HCl,反应中氢离子的物质的量不变,设加入稀硫酸的体积为xmL,利用氢离子物质的量列方程,则:
0.001mol/L×(V+x)mL=xmL×0.05mol/L×2,
解得x=
,
故答案:
mL;
②氯化钡与硫酸反应生成硫酸钡与HCl,氯化钡的物质的量等于硫酸的物质的量,令氯化钡的浓度为ymol/L,则:
ymol/L×VmL=0.05mol/L×
mL
解得 y=5.05×10-4,
答:原氯化钡溶液的物质的量浓度为5.05×10-4mol/L.
②由图可知,温度越高,混合体系中SO3的百分含量越小,说明升高温度平衡向逆反应进行,K值减小,故平衡常数K1>K2,D状态未达平衡,混合体系中SO3的百分含量小于平衡时的,反应向正反应进行建立平衡,所以V正>V逆,
故答案为:>;>;
(2)①由图可知,N2和H2反应生成1molNH3放出的热量为(Q2-Q1)kJ,该反应的热化学反应方程式为N2(g)+3H2(g)?2NH3(g)△H=-2(Q2-Q1)kJ?mol-1,
故答案为:N2(g)+3H2(g)?2NH3(g)△H=-2(Q2-Q1)kJ?mol-1.
②根据氨水的电离平衡常数为电离出离子的浓度积与溶质浓度的比值,则氨水中的电离常数为K=
| c(NH4+)?c(H+) |
| c(NH 3?H 2O) |
K=
| c(NH4+)?c(H+) |
| c(NH 3?H 2O) |
| 10 -7b |
| a-b |
故答案为:K=
| c(NH4+)?c(H+) |
| c(NH 3?H 2O) |
| 10 -7b |
| a-b |
(3)①氯化钡与硫酸反应生成硫酸钡与HCl,反应中氢离子的物质的量不变,设加入稀硫酸的体积为xmL,利用氢离子物质的量列方程,则:
0.001mol/L×(V+x)mL=xmL×0.05mol/L×2,
解得x=
| V |
| 99 |
故答案:
| V |
| 99 |
②氯化钡与硫酸反应生成硫酸钡与HCl,氯化钡的物质的量等于硫酸的物质的量,令氯化钡的浓度为ymol/L,则:
ymol/L×VmL=0.05mol/L×
| V |
| 99 |
解得 y=5.05×10-4,
答:原氯化钡溶液的物质的量浓度为5.05×10-4mol/L.
点评:本题考查化学平衡、热化学方程式及读图能力,根据方程式的计算等,难度中等,侧重对学生基础知识的考查,注意反应中氢离子、氯离子的物质的量不变,(2)中用字母表示反应热数值,符号的确定容易忽略,为易错点.

练习册系列答案
 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
下列关于油脂的说法不正确的是( )
| A、油脂属于酯类 |
| B、油脂的密度比水小,不溶于水 |
| C、油脂可分为油和脂肪 |
| D、油脂属于高分子化合物 |
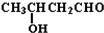
 +CO
+CO