题目内容
15. 工业上可采用电化学法利用H2S废气制取氢气,该法制氢过程的示意图所示,回答下列问题:
工业上可采用电化学法利用H2S废气制取氢气,该法制氢过程的示意图所示,回答下列问题:(1)产生反应池中发生反应的化学方程式为H2S+2FeCl3=2FeCl2+S↓+2HCl.
(2)反应后的溶液进入电解池,电解时阳极反应式为Fe2+-e-=Fe3+.
(3)若电解池中生成5.6L H2(标准状况),则理论上在反应池中可生成S沉淀的物质的量为0.25 mol.
分析 (1)反应池中加入的是硫化氢和氯化铁溶液,生成物中有S沉淀,该反应中硫化氢失电子作还原剂,则氯化铁作氧化剂,被还原生成氯化亚铁;
(2)电解氯化亚铁溶液时,阳极上亚铁离子失电子生成铁离子;
(3)反应池中转移电子数等于电解池中转移电子数,根据转移电子相等计算生成S的物质的量.
解答 解:(1)反应池中加入的是硫化氢和氯化铁溶液,生成物中有S沉淀,该反应中硫化氢失电子作还原剂,则氯化铁作氧化剂,被还原生成氯化亚铁,反应方程式为H2S+2FeCl3=2FeCl2+S↓+2HCl,故答案为:H2S+2FeCl3=2FeCl2+S↓+2HCl;
(2)电解氯化亚铁溶液时,阳极上亚铁离子失电子生成铁离子,电极反应式为Fe2+-e-=Fe3+,故答案为:Fe2+-e-=Fe3+;
(3)反应池中转移电子数等于电解池中转移电子数,n(H2)=$\frac{5.6L}{22.4L/mol}$=0.25mol,转移电子的物质的量为0.5mol,根据转移电子相等得生成n(S)=$\frac{0.5mol}{2}$=0.25mol,
故答案为:0.25.
点评 本题考查电解原理,为高频考点,涉及氧化还原反应、电极反应式的书写、物质的量的有关计算等知识点,侧重考查学生图片分析判断及计算能力,注意(1)中方程式的书写,题目难度不大.

练习册系列答案
相关题目
6.已知乙烯分子中含有一个碳碳双键,分子呈平面结构,六个原子都在同一平面上,下列对丙烯(CH3-CH═CH2)结构和性质的推断正确的是( )
| A. | 丙烯分子中所有的原子都在同一平面上 | |
| B. | 丙烯分子中三个碳原子有可能在同一条直线上 | |
| C. | 过量的丙烯通入浓溴水中,观察到溴水褪色,溶液均一稳定 | |
| D. | 丙烯既可以发生加成反应,又可以发生取代反应 |
3.下表列出了①~⑨九种元素在周期表中的位置.
请按要求回答下列问题:
(1)①~⑨九种元素中非金属性最强的是F(填元素符号).
(2)元素⑧的原子结构示意图是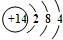 ;由①、④、⑥三种元素组成的化合物,其电子式是
;由①、④、⑥三种元素组成的化合物,其电子式是 .
.
(3)元素②、⑧的气态氢化物的稳定性较强的是CH4(填化学式);元素③、⑨的最高价氧化物对应的水化物的酸性较强的是HClO4(填化学式).
(4)③、④、⑧三种元素的原子半径由大到小的顺序是Si>N>O(填元素符号).
(5)元素⑤、⑥组成的化合物的化学键类型是离子键.
(6)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式是Al(OH)3+OH-═AlO2-+2H2O.
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(1)①~⑨九种元素中非金属性最强的是F(填元素符号).
(2)元素⑧的原子结构示意图是
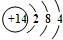 ;由①、④、⑥三种元素组成的化合物,其电子式是
;由①、④、⑥三种元素组成的化合物,其电子式是 .
.(3)元素②、⑧的气态氢化物的稳定性较强的是CH4(填化学式);元素③、⑨的最高价氧化物对应的水化物的酸性较强的是HClO4(填化学式).
(4)③、④、⑧三种元素的原子半径由大到小的顺序是Si>N>O(填元素符号).
(5)元素⑤、⑥组成的化合物的化学键类型是离子键.
(6)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式是Al(OH)3+OH-═AlO2-+2H2O.
20.下列各组离子在溶液中可以大量共存,加入足量的FeBr2晶体时,只有一种离子浓度明显减少的是( )
| A. | K+、OH-、CO32- | B. | Na+、Cl-、Ag+ | C. | K+、SO42-、S2- | D. | H+、Cu2+、NO3- |
7.下列说法中正确的是( )
| A. | 所有铵盐受热均可以分解,产物均有NH3 | |
| B. | 所有铵盐都易溶于水,不是所有铵盐中的氮均呈-3价 | |
| C. | NH4Cl溶液中加入NaOH浓溶液共热,离子方程式为NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | NH4Cl和NaCl的固体混合物,可用升华法分离 |
4.化学与社会、生产、生活密切相关.下列说法正确的是( )
| A. | 石英只能用于生产光导纤维 | |
| B. | 从海水中提取物质都必须通过化学反应才能实现 | |
| C. | 用SO2漂白纸浆和草帽辫 | |
| D. | 硅胶可作袋装食品的干燥剂 |
5.某溶液中c(H+)>c(OH-),该溶液呈( )
| A. | 中性 | B. | 酸性 | C. | 碱性 | D. | 无法判断 |