题目内容
16.在下列条件下,两种气体的分子数一定相等的是( )| A. | 同质量、同密度的O2和NO | B. | 同质量、不同密度的NO和C2H6 | ||
| C. | 同体积、同压强的CO和C2H4 | D. | 同温度、同体积的N2和O2 |
分析 根据N=nNA可知,两种气体的分子数相等,说明气体的物质的量相等,根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$分别判断各选项中两种气体的物质的量是否相等即可.
解答 解:根据N=nNA可知,两种气体的分子数相等,说明气体的物质的量相等,
A.同质量、同密度的O2和NO,二者的质量相等,由于二者的摩尔质量不同,根据n=$\frac{m}{M}$可知,二者的物质的量不相等,故A错误;
B.NO和C2H6的摩尔质量都是30g/mol,质量相等时二者的物质的量相等,含有的分子数相等,故B正确;
C.没有告诉温度,则气体摩尔体积不一定相等,无法计算二者的物质的量,故C错误;
D.没有告诉压强,无法计算二者的物质的量,故D错误;
故选B.
点评 本题考查了物质的量的计算,题目难度中等,明确气体摩尔体积的使用条件为解答关键,注意掌握物质的量与摩尔质量、阿伏伽德罗常数之间的关系,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
6.中美科学家研制的某快充电池工作原理如图所示.电解质为一种常温离子液体(由有机阳离子、Al2Cl7-和AlCl4-组成),在电池充、放电过程中,不产生其他离子且有机阳离子不参与电极反应.下列有关该快充电池的说法错误的是( )
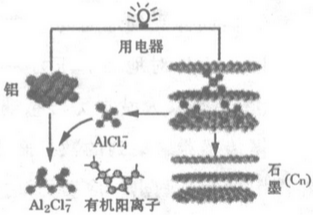

| A. | 放电时铝为电池阳极 | |
| B. | 充电时AlCl4-移向石墨电极 | |
| C. | 铝电极的比能量较高 | |
| D. | 充电时铝电极上的反应为Al+7AlCl4--3e-=4Al2Cl7- |
11.下列名称的有机物实际上不可能存在的是( )
| A. | 2,2-二甲基丁烷 | B. | 3-甲基-1-丁炔 | ||
| C. | 3-甲基-2-戊烯 | D. | 3,3-二甲基-2-戊烯 |
1.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 11.2 L Cl2与4.25 g NH3所含有的原子数一定相等 | |
| B. | 标准状况下36 g H2O与1.204×1024个O2分子所占的体积 | |
| C. | 100 mL 0.1 mol/L AlCl3溶液中,Al3+个数为0.01NA | |
| D. | 0.1 mol NH${\;}_{2}^{-}$所含电子数约为6.02×1023个 |
8.已知粗铜中含有少量的锌、铁、银、金等金属和其它杂质(杂质与酸不反应).
(1)电解精炼铜后所得的阳极泥的综合利用:
①用稀硝酸处理阳极泥得到硝酸银稀溶液,写出该步反应的离子方程式:3Ag+4H++NO3-=3Ag++NO↑+2H2O
②残渣含有极少量的黄金.经过查阅有关资料,了解到一些有关金的知识如下:
从中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与浓盐酸按体积比1:3的混合物),请简要解释金能够溶于王水的原因浓盐酸含有大量氯离子,Au3+离子与氯离子形成稳定的AuCl4-离子,使反应1平衡向右移动,则金溶于王水中
(2)电解后废液的测定:以下是该小组探究废液的一个实验流程:

①锌同铝一样,都是活泼金属,其氢氧化物既能溶于强酸生成Zn2+,又能溶于强碱生成ZnO22-.写出锌和氢氧化钠溶液反应的离子方程式Zn+2OH-+2H2O=[Zn(OH)4]2-+H2↑
②100mL废液中Cu2+的浓度为0.5mol•L-1,Fe2+的浓度为0.1mol•L-1.
(1)电解精炼铜后所得的阳极泥的综合利用:
①用稀硝酸处理阳极泥得到硝酸银稀溶液,写出该步反应的离子方程式:3Ag+4H++NO3-=3Ag++NO↑+2H2O
②残渣含有极少量的黄金.经过查阅有关资料,了解到一些有关金的知识如下:
| 序号 | 反应 | 化学平衡常数 |
| 1 | Au+6HNO3(浓)?Au(NO3)3+3NO2↑+3H2O | <<1 |
| 2 | Au3++4Cl-=AuCl4- | >>1 |
(2)电解后废液的测定:以下是该小组探究废液的一个实验流程:

①锌同铝一样,都是活泼金属,其氢氧化物既能溶于强酸生成Zn2+,又能溶于强碱生成ZnO22-.写出锌和氢氧化钠溶液反应的离子方程式Zn+2OH-+2H2O=[Zn(OH)4]2-+H2↑
②100mL废液中Cu2+的浓度为0.5mol•L-1,Fe2+的浓度为0.1mol•L-1.
5.在恒温恒容容器中进行反应A(g)?2B(g)+C(g),若A的浓度由0.1mol•L-1降到0.06mol•L-1需20s,那么由0.06mol•L-1降到0.024mol•L-1,需要时间可能是( )
| A. | 18s | B. | 12s | C. | 30s | D. | 10s |
6.下列关于金属冶炼说法正确的是 ( )
| A. | 电解铝时阴极材料需要定期更换 | |
| B. | 炼钢中添加硅、锰、铝等作为脱氧剂,调整钢水的成分,制成多种性能优良的钢材 | |
| C. | 炼钢主要目的是在高温下用还原剂将过多的碳和其他杂质还原成气体或炉渣除去 | |
| D. | 工业上一般以铁矿石、焦炭、石灰石和空气等原料在高炉中冶炼生铁 |
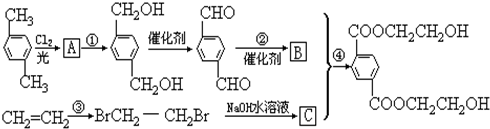
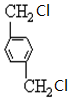 、
、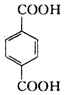 、HOCH2CH2OH.
、HOCH2CH2OH.