题目内容
现有一包铁粉和铜粉的混合粉末,为确定其组成,现提供4mol?L-1的FeCl3溶液(其他用品略),某化学小组的实验结果如表(假定反应前后溶液的体积不变):
试回答下列问题:
(1)由第②组数据计算可知,原混合粉末中n(Fe):n(Cu)= .
(2)在②、③、④中,剩余固体只有铜的是 .
(3)第①组溶液反应后,溶液中c(Fe3+)= mol?L-1.
| 组别 | ① | ② | ③ | ④ |
| V[FeCl3(aq)]/mL | 100 | 100 | 100 | 100 |
| 混合粉末的质量/g | 6 | 13.2 | 24 | 36 |
| 反应后剩余固体的质量/g | 0 | 1.28 | 12.8 | 24.8 |
(1)由第②组数据计算可知,原混合粉末中n(Fe):n(Cu)=
(2)在②、③、④中,剩余固体只有铜的是
(3)第①组溶液反应后,溶液中c(Fe3+)=
考点:有关混合物反应的计算
专题:
分析:铁的还原性强于铜,所以Fe3+先和铁发生反应:Fe+2Fe3+=3Fe2+,反应完全后,Fe3+有剩余,再与铜发生反应:Cu+2Fe3+=Fe2++Cu2+,能剩余的固体可以是铜,可以是铁和铜,由第②组数据中可以得出②中FeCl3溶液全部参与反应,100mL FeCl3溶液能溶解金属质量为13.2g-1.28g=11.92g,大于第①组溶解的金属质量,故第①组金属完全反应、FeCl3有剩余,第②组实验中FeCl3溶液全部参与反应,其物质的量为=0.1L×4mol/L=0.4mol,假设只发生:Fe+2Fe3+=3Fe2+,加反应金属的物质的量为0.2mol,则溶解的Fe的质量为0.2mol×56g/mol=11.2g<11.92g,所以同时也有一部分Cu溶解,所以剩余的固体全部为Cu;
第③组实验中溶解金属为24g-12.8g=11.2g,混合物中Fe恰好完全反应、Cu不反应,剩余12.8g为Cu;故第④组实验中,剩余固体为Fe、Cu,
(1)结合③组中Fe、Cu质量,根据n=
计算原混合粉末中n(Fe):n(Cu),
(3)计算6g混合物中Fe、Cu的物质的量,再根据方程式计算反应的Fe3+的物质的量,进而计算反应后溶液中c(Fe3+).
第③组实验中溶解金属为24g-12.8g=11.2g,混合物中Fe恰好完全反应、Cu不反应,剩余12.8g为Cu;故第④组实验中,剩余固体为Fe、Cu,
(1)结合③组中Fe、Cu质量,根据n=
| m |
| M |
(3)计算6g混合物中Fe、Cu的物质的量,再根据方程式计算反应的Fe3+的物质的量,进而计算反应后溶液中c(Fe3+).
解答:
解:铁的还原性强于铜,所以Fe3+先和铁发生反应:Fe+2Fe3+=3Fe2+,反应完全后,Fe3+有剩余,再与铜发生反应:Cu+2Fe3+=Fe2++Cu2+,能剩余的固体可以是铜,可以是铁和铜,由第②组数据中可以得出②中FeCl3溶液全部参与反应,100mL FeCl3溶液能溶解金属质量为13.2g-1.28g=11.92g,大于第①组溶解的金属质量,故第①组金属完全反应、FeCl3有剩余,第②组实验中FeCl3溶液全部参与反应,其物质的量为=0.1L×4mol/L=0.4mol,假设只发生:Fe+2Fe3+=3Fe2+,加反应金属的物质的量为0.2mol,则溶解的Fe的质量为0.2mol×56g/mol=11.2g<11.92g,所以同时也有一部分Cu溶解,所以剩余的固体全部为Cu;
第③组实验中溶解金属为24g-12.8g=11.2g,混合物中Fe恰好完全反应、Cu不反应,剩余12.8g为Cu;故第④组实验中,剩余固体为Fe、Cu,
(1)第③合金中Fe与Cu的质量分别为11.2g、12.8g,则原混合粉末中n(Fe):n(Cu)=
:
=1:1,故答案为:1:1;
(2)由上述分析可知,在②、③、④中,剩余固体只有铜的是②③,故答案为:②③;
(3)①中n(Fe)=n(Cu)=
=0.05mol,由Fe+2Fe3+=3Fe2+、Cu+2Fe3+=Fe2++Cu2+,可知反应的Fe3+为0.05mol×2+0.05mol×2=0.2mol,故第①组溶液反应后,溶液中c(Fe3+)=4mol/L-
=2mol/L,故答案为:2.
第③组实验中溶解金属为24g-12.8g=11.2g,混合物中Fe恰好完全反应、Cu不反应,剩余12.8g为Cu;故第④组实验中,剩余固体为Fe、Cu,
(1)第③合金中Fe与Cu的质量分别为11.2g、12.8g,则原混合粉末中n(Fe):n(Cu)=
| 11.2g |
| 56g/mol |
| 12.8g |
| 64g/mol |
(2)由上述分析可知,在②、③、④中,剩余固体只有铜的是②③,故答案为:②③;
(3)①中n(Fe)=n(Cu)=
| 6g |
| 56g/mol+64g/mol |
| 0.2mol |
| 0.1L |
点评:本题考查了混合物的有关计算,关键是通过②判断剩余固体为铜,题目综合性较大,数据较复杂,侧重学生对实验数据的分析处理考查,难度较大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列图示与对应的叙述相符的是( )


| A、图1表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的过饱和溶液 |
| B、图2表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| C、图3表示0.1000mol?L-1NaOH溶液滴定20.00mL0.1000mol?L-1醋酸溶液得到滴定曲线 |
| D、图4表示向NH4Al(SO4)2溶液中逐渐滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化 |
含杂质的CaCO310g和足量的盐酸反应,产生了0.1mol的CO2,则CaCO3中的杂质可能是( )
| A、MgCO3和SiO2 |
| B、MgCO3和KHCO3 |
| C、K2CO3和Na2CO3 |
| D、Na2CO3和MgCO3 |
相对分子质量为86的烷烃含碳原子数为( )
| A、6 | B、5 | C、4 | D、3 |


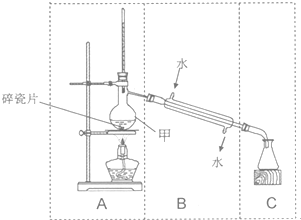
 乙醇、1,2-二溴乙烷、乙醚的有关物理性质如表所示.
乙醇、1,2-二溴乙烷、乙醚的有关物理性质如表所示.