题目内容
12.下列关于化学反应的速率和限度的说法错误的是( )| A. | 化学反应速率通过用单位时间里反应物浓度或生成物浓度的变化量表示 | |
| B. | 化学平衡状态指的是在一定条件下反应物和生成物浓度不再改变时的状态 | |
| C. | 决定化学反应速率的主要因素是温度 | |
| D. | 催化剂只能加快化学反应速率,不能提高原料利用率和转化率 |
分析 A.v=$\frac{△c}{△t}$,为平均速率;
B.化学平衡状态时浓度不变;
C.决定化学反应速率的主要因素为反应物本身的性质;
D.催化剂对化学平衡移动无影响.
解答 解:A.化学反应速率通过用单位时间里反应物浓度或生成物浓度的变化量表示,表达式为v=$\frac{△c}{△t}$,为平均速率,故A正确;
B.化学平衡状态时浓度不变,则化学平衡状态指的是在一定条件下反应物和生成物浓度不再改变时的状态,故B正确;
C.决定化学反应速率的主要因素为反应物本身的性质,而温度为影响反应速率的外界因素,故C错误;
D.催化剂对化学平衡移动无影响,则催化剂只能加快化学反应速率,不能提高原料利用率和转化率,故D正确;
故选C.
点评 本题考查化学反应速率和化学平衡的影响因素,为高频考点,把握反应速率的影响及平衡移动为解答的关键,侧重分析与应用能力的考查,注意平衡状态的理解,题目难度不大.

练习册系列答案
相关题目
2.下列原理或操作的说法正确的是( )
| A. | 吸滤既能加快过滤速率和得到更干燥的沉淀,又能使沉淀颗粒变粗变大 | |
| B. | 在“阿司匹林的合成”实验中,把从盐酸中析出的晶体进行抽滤,用酒精洗涤晶体1~2次,然后抽滤,将晶体转移到表面皿上,干燥后称其质量,计算产率 | |
| C. | 记录Na2S2O3与稀硫酸的反应时间,应从溶液混合时开始计时,到刚出现浑浊结束 | |
| D. | 硫酸亚铁铵晶体过滤后用无水乙醇洗涤而不要用水洗涤主要是为了减少晶体损失 |
3.与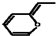 互为同分异构体的是( )
互为同分异构体的是( )
 互为同分异构体的是( )
互为同分异构体的是( )| A. |  | B. |  | C. | 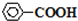 | D. |  |
20.下列各组物质中的两种物质化学键类型相同的是( )
| A. | CaCl2、HCl | B. | MgCO3、Na2S | C. | KOH、NaCl | D. | H2O、NH3 |
7. 美国魏考克斯合成的一种有机分子,像一尊释迦牟尼佛.称为释迦牟尼分子.有关该有机分子的说法正确的是( )
美国魏考克斯合成的一种有机分子,像一尊释迦牟尼佛.称为释迦牟尼分子.有关该有机分子的说法正确的是( )
 美国魏考克斯合成的一种有机分子,像一尊释迦牟尼佛.称为释迦牟尼分子.有关该有机分子的说法正确的是( )
美国魏考克斯合成的一种有机分子,像一尊释迦牟尼佛.称为释迦牟尼分子.有关该有机分子的说法正确的是( )| A. | 该有机物属于苯的同系物 | |
| B. | 1mol该有机物完全燃烧需消耗25molO2 | |
| C. | 1mol该有机物最多可以和10molH2发生加成反应 | |
| D. | 该有机物的一氯代产物的同分异构体有12种 |
17.下列有关表述错误的是( )
| A. | IBr的电子式为  | |
| B. | HClO的结构式为H-O-Cl | |
| C. | HIO各原子都满足8电子结构 | |
| D. | 共价化合物内部可能有极性键和非极性键 |
4.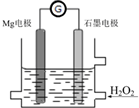 Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下.下列说法不正确的是( )
Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下.下列说法不正确的是( )
 Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下.下列说法不正确的是( )
Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下.下列说法不正确的是( )| A. | 镁电极是该电池的负极 | |
| B. | 石墨电极上发生还原反应 | |
| C. | Mg电极的电极反应式:Mg-2e-═Mg2+ | |
| D. | 电池工作时,电子从石墨电极经导线流向Mg电极,溶液中阳离子流向正极 |
1.某甲、乙两种气态烃混合物,其中甲的相对分子质量小于乙,混合气体的密度是相同状况下H2密度的13倍,把标准状况下4.48L该混合气体通入足量的溴水中,溴水增重2.8g,则下列有关叙述错误的是( )
| A. | 甲一定是烷烃 | |
| B. | 乙的物质的量为0.05mol | |
| C. | 符合条件的乙的可能结构有3种(包含顺反异构) | |
| D. | 甲的质量为2.4g |
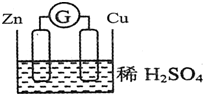 请观察如图装置,回答下列问题:
请观察如图装置,回答下列问题: