题目内容
在 700℃时,向容积为 2 L 的密闭容器中充入一定量的 CO 和 H2O,发生反应:CO(g) + H2O(g)  CO2(g)+ H2(g),反应过程中测定的部分数据见下表(表中 t2 > t1)。
CO2(g)+ H2(g),反应过程中测定的部分数据见下表(表中 t2 > t1)。
反应时间/min | n(CO)/mol | n(H2O)/mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
下列说法中正确的是
A.反应在 t1 min 内的平均反应速率为υ(CO2) =  mol/(L·min)
mol/(L·min)
B.到 t1 min 时,反应未达到平衡状态
C.温度升至 800℃时,上述反应的平衡常数为 0.64,则正反应为放热反应
D.保持 700℃不变,向平衡体系中再通入 0.60 mol CO 和 0.30 mol H2O,达到新的平衡,与原平衡相比,CO的转化率增大,H2 的体积分数增大
练习册系列答案
相关题目


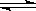 N2(g)+S(l)+4H2O(g) ΔH﹤0 。下列有关说法正确的是
N2(g)+S(l)+4H2O(g) ΔH﹤0 。下列有关说法正确的是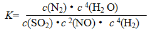
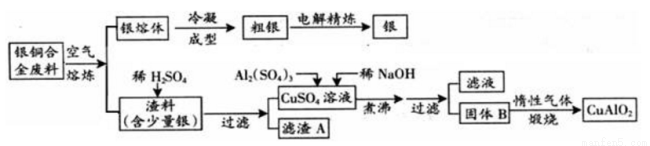
 CuAlO2+ ↑。
CuAlO2+ ↑。
 =___________。
=___________。
