题目内容
1.K2SO4是无氯优质钾肥,Mn3O4是生产软磁铁氧体材料的主要原料.以硫酸工业的尾气联合制备K2SO4和Mn3O4的工艺流程如图1: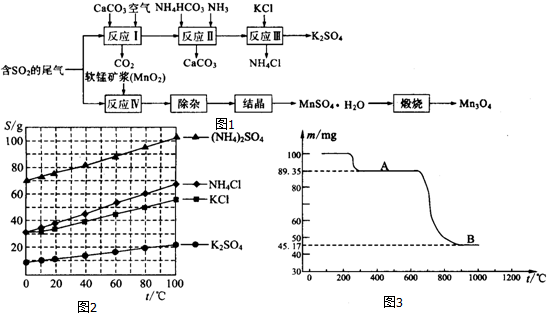
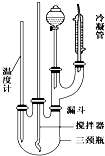
(1)几种盐的溶解度见图2.反应Ⅲ中,向(NH4)2SO4溶液中加入KCl溶液充分反应后,进行蒸发浓缩、趁热过滤、洗涤、干燥等操作即得K2SO4产品.
(2)检验K2SO4样品是否含有氯化物杂质的实验操作是取少量溶液于试管中配成溶液,滴加过量的Ba(NO3)2溶液,取上层清液滴加AgNO3溶液.
(3)反应Ⅳ的化学方程式为MnO2+SO2=MnSO4.
(4)Mn3O4与浓盐酸加热时发生反应的离子方程式为Mn3O4+8H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$3Mn2++Cl2↑+4H2O.
(5)图3煅烧MnSO4•H2O时温度与剩余固体质量变化曲线.
①该曲线中B段所表示物质的化学式为Mn3O4.
②煅烧过程中固体锰含量随温度的升高而增大,但当温度超过1000℃时,再冷却后,测得产物的总锰含量反而减小.试分析产物总锰含量减小的原因部分Mn3O4又被氧化成Mn2O3或MnO2,造成总锰含量减少.
分析 (1)硫酸钾的溶解度受温度的影响较小,趁热过滤减少杂质;
(2)检验Cl-用硝酸银溶液和稀硝酸,同时又要除去干扰实验的硫酸根离子;
(3)二氧化硫与二氧化锰反应,除杂后得到硫酸锰晶体,可知二者反应生成硫酸锰;
(4)+4价锰离子具有氧化性可以氧化氯离子为氯气,四氧化三锰可改写为MnO2•2MnO,MnO2与浓盐酸生成MnCl2、Cl2和H2O、MnO与盐酸生成MnCl2和H2O;
(5)热重曲线中一般先失去结晶水(可能分步),100gMnSO4•H2O中结晶水的质量为100g×$\frac{18}{55+96+18}$=10.65g,可知A为硫酸锰,升高温度盐分解得到金属氧化物,由流程图可知硫酸锰晶体锻烧得到四氧化三锰,100gMnSO4•H2O分解可以得到四氧化三锰的质量为$\frac{100g}{(55+96+18)g/mol}$×$\frac{1}{3}$×229g/mol=45.17g,故B为Mn3O4;继续加热产物中总锰含量反而减小,说明吸收了氧,进一步说明B中的锰元素存在低价.
解答 解:(1)四种物质中相同温度下硫酸钾溶解度最小,所以反应Ⅲ中蒸发浓缩后硫酸钾析出,趁热过滤减少杂质,得硫酸钾晶体,再洗涤、干燥即可,
故答案为:趁热过滤;
(2)检验Cl-用硝酸银溶液和稀硝酸,同时又要除去干扰实验的硫酸根离子,具体方案为:取少量溶液于试管中配成溶液,滴加过量的Ba(NO3)2溶液,取上层清液滴加AgNO3溶液,
故答案为:取少量溶液于试管中配成溶液,滴加过量的Ba(NO3)2溶液,取上层清液滴加AgNO3溶液;
(3)二氧化硫与二氧化锰反应,除杂后得到硫酸锰晶体,可知二者反应生成硫酸锰,反应方程式为:MnO2+SO2=MnSO4,
故答案为:MnO2+SO2=MnSO4;
(4)+4价锰离子具有氧化性可以氧化氯离子为氯气,四氧化三锰可改写为MnO2•2MnO,MnO2与浓盐酸生成MnCl2、Cl2和H2O、MnO与盐酸生成MnCl2和H2O,反应方程式为:Mn3O4+8H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$3Mn2++Cl2↑+4H2O,
故答案为:Mn3O4+8H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$3Mn2++Cl2↑+4H2O;
(5)①热重曲线中一般先失去结晶水(可能分步),100gMnSO4•H2O中结晶水的质量为100g×$\frac{18}{55+96+18}$=10.65g,可知A为硫酸锰,升高温度盐分解得到金属氧化物,由流程图可知硫酸锰晶体锻烧得到四氧化三锰,100gMnSO4•H2O分解可以得到四氧化三锰的质量为$\frac{100g}{(55+96+18)g/mol}$×$\frac{1}{3}$×229g/mol=45.17g,故B为Mn3O4,
故答案为:Mn3O4;
②继续加热产物中总锰含量反而减小,说明吸收了氧,进一步说明B中的锰元素存在低价,可能是部分Mn3O4又被氧化成Mn2O3或MnO2,造成总锰含量减少,
故答案为:部分Mn3O4又被氧化成Mn2O3或MnO2,造成总锰含量减少.
点评 本题考查物质制备工艺流程、离子检验、陌生方程式书写、物质的分离提纯、化学反应图象等,(5)中注意利用验证法解答,避免计算确定B的化学式中繁琐数据处理.

| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O ? CO2 | ||
| C. | NH3 H2O CO2 | D. | CaCl2 ? NaOH H2O |
(1)上述实验中发生反应的化学方程式有CuSO4+Zn═ZnSO4+Cu,Zn+H2SO4═ZnSO4+H2↑;
(2)硫酸铜溶液可以加快氢气生成速率的原因是CuSO4与Zn反应产生的Cu与Zn可形成Cu-Zn原电池,加快了氢气产生的速率;
(3)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是Ag2SO4;
(4)要加快上述实验中气体产生的速率,还可采取的措施有升高反应温度、适当增加硫酸的浓度、增加锌粒的表面积等(答两种);
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
②该同学最后得出的结论为当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因当加入一定量的CuSO4后,生成的单质Cu会沉积在Zn的表面,降低了Zn与H2SO4溶液的接触面积而使反应速率下降.
| X | Y | W | Z | 反应体系能量变化 | |
| 甲 | 2mol | 1mol | 放出akJ/mol | ||
| 乙 | 1mol | 1mol | 放出bkJ/mol | ||
| 丙 | 2mol | 2mol | 放出ckJ/mol | ||
| 丁 | 3mol | 2mol | 吸收dkJ/mol |
| A. | c+d<Q | |
| B. | 平衡时,甲、丁容器中X、W的转化率之和大于1 | |
| C. | 平衡时丙容器中Z的物质的量浓度最大 | |
| D. | X的转化率为:甲<乙<丙 |
| 元素符号 | 元素性质或原子结构 |
| T | M层上的电子数是原子核外电子层数的2倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
| A. | 14X可用与测定文物年代 | B. | Z的非金属性比T强 | ||
| C. | Y和T位于同一主族 | D. | X元素形成的化合物种类很多 |
 硝基苯是一种重要的化工原料,其制备原理是:
硝基苯是一种重要的化工原料,其制备原理是: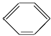 +HO-NO2$→_{50~60℃}^{H_{2}SO_{4}}$
+HO-NO2$→_{50~60℃}^{H_{2}SO_{4}}$ 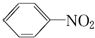 +H2O△H<0
+H2O△H<0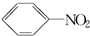 +HO-NO2$→_{△}^{H_{2}SO_{4}}$
+HO-NO2$→_{△}^{H_{2}SO_{4}}$ 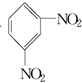 +H2O
+H2O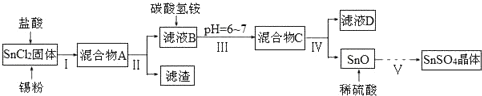
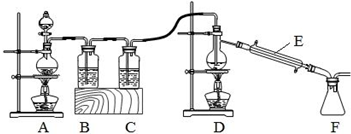
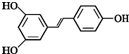 .根据要求回答下列问题:
.根据要求回答下列问题: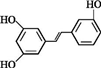 .
.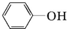 )都含有与白藜芦醇相同的官能团,有关它们之间关系的说法正确的是C.
)都含有与白藜芦醇相同的官能团,有关它们之间关系的说法正确的是C.