题目内容
下列有关表述正确的是( )
①-OH与 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同
②HCN分子的结构式:H-C≡N
③Br-的离子结构示意图:
④CO2的分子模型示意图:
⑤丙烷分子的球棍模型:
⑥次氯酸的电子式为:
⑦ 的名称为:1,3-二甲基-2-丁烯
的名称为:1,3-二甲基-2-丁烯
⑧熔化时NaHSO4的电离方程式为:NaHSO4=Na++HSO4-.
①-OH与
 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同 ②HCN分子的结构式:H-C≡N
③Br-的离子结构示意图:

④CO2的分子模型示意图:

⑤丙烷分子的球棍模型:

⑥次氯酸的电子式为:

⑦
 的名称为:1,3-二甲基-2-丁烯
的名称为:1,3-二甲基-2-丁烯⑧熔化时NaHSO4的电离方程式为:NaHSO4=Na++HSO4-.
| A、①②④⑥ | B、①④⑤⑧ |
| C、①②⑤⑧ | D、②③⑤⑦ |
考点:电子式、化学式或化学符号及名称的综合,原子结构示意图,电离方程式的书写,球棍模型与比例模型
专题:
分析:①-OH与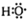 分别为羟基的结构简式和电子式;
分别为羟基的结构简式和电子式;
②书写结构简式时注意C≡N三键不能省略;
③溴离子的核电荷数为35;
④二氧化碳为直线型结构;
⑤丙烷为饱和烷烃,存在碳碳单键和碳氢单键,四个碳原子在一条连上;
⑥次氯酸中氧原子分别与氯原子和氢原子共用1对电子;
⑦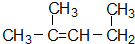 最长碳链为5个碳原子,从右端开始编号,2号碳上有1个甲基和双键,据此命名;
最长碳链为5个碳原子,从右端开始编号,2号碳上有1个甲基和双键,据此命名;
⑧熔化时NaHSO4的时候,只电离出钠离子与硫酸氢根离子.
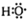 分别为羟基的结构简式和电子式;
分别为羟基的结构简式和电子式;②书写结构简式时注意C≡N三键不能省略;
③溴离子的核电荷数为35;
④二氧化碳为直线型结构;
⑤丙烷为饱和烷烃,存在碳碳单键和碳氢单键,四个碳原子在一条连上;
⑥次氯酸中氧原子分别与氯原子和氢原子共用1对电子;
⑦
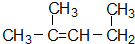 最长碳链为5个碳原子,从右端开始编号,2号碳上有1个甲基和双键,据此命名;
最长碳链为5个碳原子,从右端开始编号,2号碳上有1个甲基和双键,据此命名;⑧熔化时NaHSO4的时候,只电离出钠离子与硫酸氢根离子.
解答:
解:①-OH与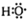 分别为羟基的结构简式和电子式,组成元素相同,含有的电子数也相同,故①正确;
分别为羟基的结构简式和电子式,组成元素相同,含有的电子数也相同,故①正确;
②HCN分子中存在C-H和C≡N,其结构式为:H-C≡N,故②正确;
③溴离子的核电荷数为35,核外电子总数为36,其正确的离子结构示意图为: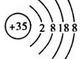 ,故③错误;
,故③错误;
④二氧化碳为直线型结构,其正确的比例模型为: ,故④错误;
,故④错误;
⑤丙烷为饱和烷烃,存在碳碳单键和碳氢单键,四个碳原子在一条连上,丙烷的球棍模型为: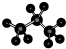 ,故⑤正确;
,故⑤正确;
⑥次氯酸的中心原子为O原子,次氯酸正确的电子式为: ,故⑥错误;
,故⑥错误;
⑦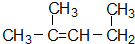 的正确名称为:2-甲基-2-戊烯,故⑦错误;
的正确名称为:2-甲基-2-戊烯,故⑦错误;
⑧熔化时NaHSO4的电离方程式为:NaHSO4═Na++HSO4-,故⑧正确;
故选C.
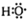 分别为羟基的结构简式和电子式,组成元素相同,含有的电子数也相同,故①正确;
分别为羟基的结构简式和电子式,组成元素相同,含有的电子数也相同,故①正确;②HCN分子中存在C-H和C≡N,其结构式为:H-C≡N,故②正确;
③溴离子的核电荷数为35,核外电子总数为36,其正确的离子结构示意图为:
 ,故③错误;
,故③错误;④二氧化碳为直线型结构,其正确的比例模型为:
 ,故④错误;
,故④错误;⑤丙烷为饱和烷烃,存在碳碳单键和碳氢单键,四个碳原子在一条连上,丙烷的球棍模型为:
 ,故⑤正确;
,故⑤正确;⑥次氯酸的中心原子为O原子,次氯酸正确的电子式为:
 ,故⑥错误;
,故⑥错误;⑦
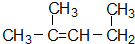 的正确名称为:2-甲基-2-戊烯,故⑦错误;
的正确名称为:2-甲基-2-戊烯,故⑦错误;⑧熔化时NaHSO4的电离方程式为:NaHSO4═Na++HSO4-,故⑧正确;
故选C.
点评:本题考查了化学用语的判断,属于基础知识的考查,题目难度中等,注意掌握常见有机物的表示方法,试题考查了学生规范答题的能力.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性比Z的气态氢化物的稳定性强,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性.下列说法正确的是( )
| A、W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 |
| B、若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
| C、X、Y、Z、W的原子半径依次减小 |
| D、W与X形成的化合物中只含离子键 |
下列性质既可能是胶体所具有,也可能是溶液所具有的是( )
| A、光线照射时,从侧面可观察到一条光亮的通路 |
| B、加入稀硫酸立即产生沉淀 |
| C、分散质粒子小于1nm |
| D、装入半透膜袋中并将其浸入盛水的烧杯中一段时间,袋内外均含分散质粒子 |
向明矾溶液中滴入Ba(OH)2溶液,当SO42-沉淀完全时,铝元素的存在形式是( )
| A、Al(OH)3和Al3+ |
| B、Al(OH)3和AlO2- |
| C、全部为Al(OH)3 |
| D、全部为AlO2- |
下列分子式能代表纯净物的是( )
| A、C4H10 |
| B、CH4O |
| C、C2H4Cl2 |
| D、C2H4O2 |
下列关于物质所属类别的叙述中正确的是( )
| A、盐类物质一定含有金属离子 |
| B、NaCl固体属于电解质 |
| C、氢氧化铁胶体、硫酸铜溶液都属于介稳体系 |
| D、凡能电离出H+的化合物均为酸 |
下列物质全部属于纯净物的是( )
| A、福尔马林、白酒、食醋 |
| B、甘油、氯仿、乙醇钠 |
| C、苯、汽油、无水乙醇 |
| D、二氯乙烷、聚氯乙烯、苯酚 |