题目内容
室温下,下列溶液中粒子浓度大小关系正确的是( )
A、NaHCO3 溶液:c(Na+)>c(HCO
| ||||
B、Na2C2O4 溶液中:c(OH-)=c(H+)+c(HC2O
| ||||
C、Na2CO3溶液:c(Na+)+c(H+)=2c(CO
| ||||
| D、CH3COONa和CH3COOH混合溶液:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
考点:离子浓度大小的比较
专题:盐类的水解专题
分析:A、碳酸氢钠溶液中碳酸氢根离子水解大于碳酸氢根离子电离,溶液呈碱性;
B、依据溶液中质子守恒分析判断;
C、结合碳酸钠溶液中电荷守恒分析判断;
D、结合电荷守恒分析判断.
B、依据溶液中质子守恒分析判断;
C、结合碳酸钠溶液中电荷守恒分析判断;
D、结合电荷守恒分析判断.
解答:
解:A、碳酸氢钠溶液中碳酸氢根离子水解大于碳酸氢根离子电离,溶液呈碱性,溶液中离子浓度c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-),故A正确;
B、Na2C2O4 溶液中质子守恒,水电离出氢氧根离子和氢离子相同:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4),故B错误;
C、Na2CO3溶液中存在电荷守恒:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-),故C错误;
D、CH3COONa和CH3COOH混合溶液中存在电荷守恒:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),若c(CH3COO-)>c(Na+),c(OH-)<c(H+),故D错误;
故选A.
B、Na2C2O4 溶液中质子守恒,水电离出氢氧根离子和氢离子相同:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4),故B错误;
C、Na2CO3溶液中存在电荷守恒:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-),故C错误;
D、CH3COONa和CH3COOH混合溶液中存在电荷守恒:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),若c(CH3COO-)>c(Na+),c(OH-)<c(H+),故D错误;
故选A.
点评:本题考查了电解质溶液中电荷守恒,物料守恒的分析判断,盐类水解分析应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
苯环结构中不存在C-C单键与C=C双键的交替结构,可以作为证据的是( )
①苯不能因反应使溴水褪色
②苯不能使酸性高锰酸钾溶液褪色
③苯在一定条件下既能发生取代反应,又能发生加成反应
④经测定,邻二甲苯只有一种结构
⑤经测定,苯环上碳碳键的键长相等.
①苯不能因反应使溴水褪色
②苯不能使酸性高锰酸钾溶液褪色
③苯在一定条件下既能发生取代反应,又能发生加成反应
④经测定,邻二甲苯只有一种结构
⑤经测定,苯环上碳碳键的键长相等.
| A、①②③⑤ | B、①②④⑤ |
| C、①②③ | D、①② |
生活中的下列物品或设备:①水泥路面;②玻璃门窗;③水晶镜片;④石英钟表;⑤玛瑙手镯;⑥太阳能电池;⑦光导纤维;⑧计算机芯片.所用材料不是SiO2的是( )
| A、⑥⑧ | B、⑤⑥⑧ |
| C、③⑤⑥⑦⑧ | D、全部 |
Na2O2、CaC2都能与水反应,且反应中都有气体放出.下列说法正确的是( )
| A、都属于氧化还原反应 |
| B、生成的气体均为氧化产物 |
| C、反应均放热 |
| D、阳离子与阴离子个数比均为1:1 |
NH3的共轭酸是( )
| A、NH4+ |
| B、NH2- |
| C、NH2- |
| D、HCONH2 |
下列实验装置或操作(已略去部分夹持仪器)正确的是( )
A、 配置溶液 |
B、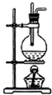 实验室制乙烯 |
C、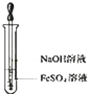 制备Fe(OH)2 |
D、 制备与收集氨气 |
体积不变的密闭容器中的可逆反应:2NO2?2NO+O2,恒温条件下,能说明反应达到平衡状态的是( )
| A、单位时间内生成n mol O2的同时生成2n mol NO |
| B、υ (NO2)=υ (NO)的状态 |
| C、混合气体的密度不变的状态 |
| D、混合气体的平均相对分子质量不再改变的状态 |
下列各组离子能够大量共存的是( )
| A、K+、Al3+、Cl-、AlO2- |
| B、Fe2+、Mg2+、SO42-、NO3- |
| C、Fe3+、K+、SO42-、S2- |
| D、Na+、Ca2+、OH-、HCO3- |