题目内容
恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示.

已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ/mol.
请回答下列问题:
(1)写出能表示硫燃烧的热化学方程式: .
(2)△H2= .
(3)恒容条件下,下列措施中能使n(SO3)/n(SO2)增大的有 .
a.升高温度 b.充入He气
c.再充入1mol SO2(g)和1mol O2(g) d.使用催化剂
(4)某SO2(g)和O2 (g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2 (g)的量,则图中t4时引起平衡移动的条件可能是 ;图中表示平衡混合物中SO3的含量最高的一段时间是 .
(5)工业排放大量的SO2气体严重污染空气,有学者想利用以下的电化学原理除去SO2的污染,同时生产有用物质.
①用惰性电极电解SO2水溶液:H2SO3
O2↑+S↓+H2O,装置如图3所示,a极连接电源的 (填“正极”或“负极”)b电极的电极反应式 ,不考虑溶液体积的变化,电解槽右池的pH将
(填“上升”、“降低”或“不变”)
②如图4所示装置用原电池原理将SO2转化为重要的化工原料.其负极的反应式为 .

已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ/mol.
请回答下列问题:
(1)写出能表示硫燃烧的热化学方程式:
(2)△H2=
(3)恒容条件下,下列措施中能使n(SO3)/n(SO2)增大的有
a.升高温度 b.充入He气
c.再充入1mol SO2(g)和1mol O2(g) d.使用催化剂
(4)某SO2(g)和O2 (g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2 (g)的量,则图中t4时引起平衡移动的条件可能是
(5)工业排放大量的SO2气体严重污染空气,有学者想利用以下的电化学原理除去SO2的污染,同时生产有用物质.
①用惰性电极电解SO2水溶液:H2SO3
| ||
(填“上升”、“降低”或“不变”)
②如图4所示装置用原电池原理将SO2转化为重要的化工原料.其负极的反应式为
考点:化学平衡的影响因素,有关反应热的计算,原电池和电解池的工作原理
专题:
分析:(1)燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物放出的热量;
(2)根据热化学方程式:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1计算;
(3)根据平衡移动判断;
恒温恒容时,开始为1molSO2和2molO2 与开始为1molSO2和1molO2 相比,开始为1molSO2和2molO2 的SO2转化率高;
(4)t2~t3段正逆速率都加快,且v(正)>v(逆),平衡正向移动,t4~t5段正逆速率都加快,且v(正)<v(逆),平衡逆向移动,该反应为体积减小的放热反应,若升高温度,平衡逆向移动,若增大压强,平衡正向移动,故t2~t3段为增大压强,t4~t5段为升高温度,t2~t3段为增大压强后,平衡正向移动,SO3的含量升高,至t3~t4平衡时含量达最高;
(5)依据电池反应负极是失去电子,发生氧化反应,阳极上是氢氧根离子失电子生成氧气的反应,据此解答即可.
(2)根据热化学方程式:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1计算;
(3)根据平衡移动判断;
恒温恒容时,开始为1molSO2和2molO2 与开始为1molSO2和1molO2 相比,开始为1molSO2和2molO2 的SO2转化率高;
(4)t2~t3段正逆速率都加快,且v(正)>v(逆),平衡正向移动,t4~t5段正逆速率都加快,且v(正)<v(逆),平衡逆向移动,该反应为体积减小的放热反应,若升高温度,平衡逆向移动,若增大压强,平衡正向移动,故t2~t3段为增大压强,t4~t5段为升高温度,t2~t3段为增大压强后,平衡正向移动,SO3的含量升高,至t3~t4平衡时含量达最高;
(5)依据电池反应负极是失去电子,发生氧化反应,阳极上是氢氧根离子失电子生成氧气的反应,据此解答即可.
解答:
解:(1)燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物放出的热量,所以,硫的物质的量为1mol.由图1可知1molS(s)完全燃烧放出的热量为297KJ,所以,硫的燃烧热的热化学方程式S(s)+O2(g)═SO2(g)△H=-297 kJ?mol-1,故答案为:S(s)+O2(g)═SO2(g)△H=-297 kJ?mol-1
(2)由由图1可知,参加反应的n(SO2)=1mol-0.2mol=0.8mol,根据热化学方程式:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1;可知,△H2=0.4△H=0.4×(=-196.6KJ?mol-1)=-78.64kJ?mol-1,故答案为:-78.64kJ?mol-1;
(3)a、反应为放热反应,温度升高,平衡逆向移动,n(SO3)减小,n(SO2)增大,n(SO3)/n(SO2)减小,故a错误;
b、恒容条件下,充入氦气,反应混合物浓度不变,平衡不移动,n(SO3)/n(SO2)不变,故b错误;
c、再充入1molSO2(g)和1molO2 (g),等效为Ⅱ压强增大一倍,平衡正向移动,n(SO3)/n(SO2)增大,故c正确;
d、使用催化剂,加快反应,平衡不移动,n(SO3)/n(SO2)不变,故d错误,故答案为:c;
(4)t2~t3段正逆速率都加快,且v(正)>v(逆),平衡正向移动.t4~t5段正逆速率都加快,且v(正)<v(逆),平衡逆向移动.该反应为体积减小的放热反应,若升高温度,平衡逆向移动,若增大压强,平衡正向移动,故t2~t3段为增大压强,t4~t5段为升高温度;t2~t3段为增大压强后,平衡正向移动,SO3的含量升高,至t3~t4平衡时含量达最高,故答案为:升高温度;t3~t4;
(5)①电池反应阳极上是氢氧根离子失电子生成氧气的反应,电极反应为:4OH--4e-═2H2O+O2↑,亚硫酸在阴极被还原为硫单质阴极,依据电极反应方程式判断得出,随着反应的进行,pH值降低,故答案为:负极;4OH--4e-═2H2O+O2↑;降低;
②二氧化硫失去电子生成硫酸根,电极方程式为:SO2+2H2O-2e-=SO42-+4H+.
(2)由由图1可知,参加反应的n(SO2)=1mol-0.2mol=0.8mol,根据热化学方程式:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1;可知,△H2=0.4△H=0.4×(=-196.6KJ?mol-1)=-78.64kJ?mol-1,故答案为:-78.64kJ?mol-1;
(3)a、反应为放热反应,温度升高,平衡逆向移动,n(SO3)减小,n(SO2)增大,n(SO3)/n(SO2)减小,故a错误;
b、恒容条件下,充入氦气,反应混合物浓度不变,平衡不移动,n(SO3)/n(SO2)不变,故b错误;
c、再充入1molSO2(g)和1molO2 (g),等效为Ⅱ压强增大一倍,平衡正向移动,n(SO3)/n(SO2)增大,故c正确;
d、使用催化剂,加快反应,平衡不移动,n(SO3)/n(SO2)不变,故d错误,故答案为:c;
(4)t2~t3段正逆速率都加快,且v(正)>v(逆),平衡正向移动.t4~t5段正逆速率都加快,且v(正)<v(逆),平衡逆向移动.该反应为体积减小的放热反应,若升高温度,平衡逆向移动,若增大压强,平衡正向移动,故t2~t3段为增大压强,t4~t5段为升高温度;t2~t3段为增大压强后,平衡正向移动,SO3的含量升高,至t3~t4平衡时含量达最高,故答案为:升高温度;t3~t4;
(5)①电池反应阳极上是氢氧根离子失电子生成氧气的反应,电极反应为:4OH--4e-═2H2O+O2↑,亚硫酸在阴极被还原为硫单质阴极,依据电极反应方程式判断得出,随着反应的进行,pH值降低,故答案为:负极;4OH--4e-═2H2O+O2↑;降低;
②二氧化硫失去电子生成硫酸根,电极方程式为:SO2+2H2O-2e-=SO42-+4H+.
点评:本题考查热化学方程式、化学平衡、电化学知识等,综合性高,难度大,关键在于读图获取信息,培养学生分析问题解决问题能力.

练习册系列答案
相关题目
2014年“世界水日”和“世界水周”的活动主题为“加强合乎管理,建设生态文明”下列关于水的说法正确的是( )
| A、为了保护水资源,禁止使用化肥 |
| B、用电解大量水的方法获得清洁能源氧气 |
| C、4℃时,纯水的pH=7 |
| D、城市浇花,采用喷灌、滴滴灌技术 |
下列叙述正确的是( )
| A、氯气的水溶液可以导电,氯气是电解质 |
| B、在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+ )增大 |
| C、升高温度,可逆反应的化学平衡常数一定增大 |
| D、在 CH3COONa 溶液中加入适量 CH3COOH,可使 c( Na+)=c(CH3COO-) |
下列有关物质与应用的对应关系正确的是( )
| A、甲醛可以使蛋白质变性,所以福尔马林可作食品的保鲜剂 |
| B、Cl2和SO2都具有漂白性,所以都可以使滴有酚酞的NaOH溶液褪色 |
| C、碳酸氢钠溶液具有弱碱性,可用于制胃酸中和剂 |
| D、氧化铝是强电解质,可电解其水溶液获得金属铝 |
通常用来衡量一个国家的石油化学工业发展水平标志的是( )
| A、石油产量 |
| B、乙烯的产量 |
| C、合成纤维的产量 |
| D、硫酸的产量 |
下列分子中所有原子都满足最外层8电子稳定结构的是( )
| A、N2 |
| B、PCl5 |
| C、BF3 |
| D、H2O |
下列醇中既能发生消去反应,又能被氧化为酮的是( )
①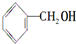 ②
② ③CH3OH④
③CH3OH④ ⑤
⑤ ⑥
⑥
①
 ②
② ③CH3OH④
③CH3OH④ ⑤
⑤ ⑥
⑥
| A、①④⑤ | B、②④⑥ |
| C、②⑥ | D、①②⑥ |
为探究锌与稀硫酸的反应速率(以v(H2)表示),向反应混合液中加入某些物质,下列判断正确的是( )
| A、加入NH4HSO4固体,v(H2)增大 |
| B、加入少量水,v(H2)不变 |
| C、加入CH3COONa固体,v(H2)减小 |
| D、滴加少量CuSO4溶液,v(H2)减小 |
化学与生产、生活息息相关,下列叙述错误的是( )
| A、为防止电池中的重金属污染土壤和水体,应积极开发废旧电池的综合回收利用 |
| B、“玉兔”月球车太阳能电池帆板的材料是二氧化硅 |
| C、大量的汽车尾气是造成雾霾天气的一个重要因素 |
| D、煤的液化和气化均属于化学变化 |