题目内容
8.页岩气是蕴藏于页岩层中的天然气,我州页岩气蕴藏量达4.81万亿立方米,约占全省近7成,可采储量超过1.443万亿立方米.页岩气将是我州能源开发的重要方向.下列有关结论中错误的是( )| A. | 页岩气是一种清洁的能源 | |
| B. | 使用页岩气是对化学能的充分利用 | |
| C. | 使用页岩气给农民的生活带来了不便 | |
| D. | 页岩气是我州解决能源的重要途径 |
分析 页岩气是蕴藏于页岩层中的天然气,而天然气的主要成分为甲烷,燃烧生成二氧化碳和水,可以将化学能转化为热能,据此分析.
解答 解:A、页岩气的主要成分为甲烷,燃烧生成二氧化碳和水,故是清洁能源,故A正确;
B、使用页岩气能将化学能转化为热能,故能对化学能进行充分利用,故B正确;
C、页岩气的使用能减少污染,且能为人民提供能量,故为人民的生活带来了很大的便利,故C错误;
D、使用页岩气能减少煤和石油的使用,故是解决能源的重要途径,故D正确.
故选C.
点评 本题考查了页岩气的主要成分以及利用问题,难度不大,应注意的是天然气是清洁能源.

练习册系列答案
相关题目
18.短周期元素X、Y、Z、W原子序数依次增大,它们原子的最外层电子数之和为14.X与Z同主族,Y与W同主族,且X的原子半径小于Y.下列叙述正确的是( )
| A. | 原子半径:Y<Z<W | |
| B. | Z在化合物中呈+1价 | |
| C. | Y与W可形成离子化合物 | |
| D. | W的单质能在Y的单质中燃烧生成WY3 |
3.下表中给出几种氯化物的熔点和沸点:
有关表中所列四种氯化物的性质,有以下叙述:①氯化铝在加热时能升华,②四氯化硅在晶态时属于分子晶体,③氯化钠晶体中微粒间以分子间作用力结合,④氯化铝晶体是典型的离子晶体,其中与表中数据一致的是:(依据晶体的性质和题给数据来分析)( )
| NaCl | MgCl2 | AlCl3 | SiCl4 | |
| 熔点(℃) | 801 | 714 | 190 | -70 |
| 沸点(℃) | 1413 | 1412 | 180 | 57.57 |
| A. | ①② | B. | ②③ | C. | ①②③ | D. | ②③④ |
13.某溶液可能含有K+、Na+、SO42-、AlO2-、NO3-、I-、Fe2+、Al3+、SiO32-.现进行如下实验:由此可知原溶液中( )
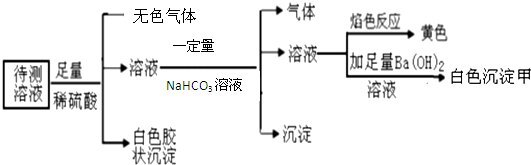

| A. | 一定含有Na+,可能存在K+ | |
| B. | 至少存在4种离子 | |
| C. | 无色气体是NO气体 | |
| D. | 白色沉淀甲中一定含有BaSO4和BaCO3 |
20.将标准状况下2.24L CO2缓慢通入100mL1.5mol•L-1NaOH溶液中(溶液体积变化忽略不计),充分反应后,下列关系正确的是( )
| A. | c(Na+)>c(CO32-)>c(HCO3-) | |
| B. | c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) | |
| C. | c(Na+)>c(HCO3-)>c(H+)>c(OH-) | |
| D. | c(HCO3-)+2c(CO32-)+c(H2CO3)=1 mol•L-1 |
18.以下表示氦原子结构的化学用语中,对电子运动状态描述最详细的是( )
| A. | :He | B. | 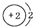 | C. | 1s2 | D. | 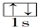 |
 .
. .
. .
.